Изучение токсического действия кислорода имеет важное практическое значение для космической медицины и биологии. Это связано с тем, что ИГА кабин космических кораблей может иметь Р О2 более высокое, чем атмосферный воздух.
Применение повышенных величин Р О2 обусловлено стремлением использовать в качестве ИГА технически наиболее удобную мо-ногазовую среду с достаточно высоким для профилактики ВДВ давлением и с некоторым резервом О2, необходимым в случаях повышенной утечки газа из кабины. Примером сказанного является ИГА космических кораблей («Меркурий», «Джемини», «Аполлон»), в которой Р О2 составляет 258 мм рт. ст. Следует также иметь в виру, что в определенный период полета Р О2 в ИГА может быть преднамеренно значительно повышено, например, перед переходом экипажа в условия ИГА с более низкпм барометрическим давлением с целью десатурации организма от N2 или какого-нибудь инертного газа. Кроме того, помимо планируемого использования повышенного Р О2 в ИГА, нельзя также полностью исключить и ситуации, когда рост Р О2 в ИГА может быть следствием неисправной работы регенерационной установки.
Для космической биологии и медицины интерес представляют в основном исследования, в которых токсическое действие О2 изучалось при нормальном или пониженном барометрическом давлении, так как вряд ли в кабинах космических кораблей будет поддерживаться барометрическое давление, значительно превышающее нормальное атмосферное.
Касаясь истории изучения токсического действия О2 на живые организмы, следует заметить, что один из первооткрывателей О2 Д. Пристли уже знал или догадывался о токсическом его действии. В 1775 г. Пристли писал: «...что хотя дефлогистированный воздух и может быть весьма полезен в качестве лекарства, он вовсе не будет столь же подходящим для нас при обычном здоровом состоянии тела: подобно тому, как свеча сгорает гораздо быстрее в дефлогистированном воздухе, чем в обычном, так и мы можем прожить слишком быстро и жизненные силы будут слишком скоро израсходованы в этом очищенном воздухе».
В 1878 г. П. Вер опубликовал книгу, в которой были представлены многочисленные экспериментальные данные о влиянии высоких концентраций О2 на живые организмы. Этот выдающийся исследователь пришел к заключению, что О2 в высоких концентрациях является «общепротоплазматическим» ядом, оказывающим токсическое действие на клетки растений и животных. В дальнейшем гипотеза П. Вера получила подтверждение в работах многих исследователей. Несмотря на многолетнее изучение токсического действия О2, информация о биохимических изменениях, определяющих развитие различных симптомов кислородной интоксикации, до сих пор остается еще недостаточной. Чанс отметили изменения окислительно-восстановительного состояния редуцированного ядерного пиридина и энергетического пути восстановления пи-ридиннуклеотида в митохондриях печени крыс и сердца морских свинок.
Многие исследователи полагают, что окисление ферментов или коферментов, содержащих SH-группы, играет важную роль в механизме токсического влияния О2 на клеточном уровне. С этим, в частности, пытаются связать раннее повреждение при гипероксии клеточных мембран.
Было отмечено, что эксперименты, в которых in vitro происходила инактивация ферментов, содержащих SH-группы, таких, как сукциндегидрогеназа, не всегда подтверждаются исследованиями, проведенными in vivo. По-видимому, большинство ферментов в организме защищено от токсического действия О2 своими субстратами-коферментами и рядом других веществ, постоянно находящихся в клетках. До сих пор остается неясным, включает ли механизм токсического действия О2 на клетку влияние самих молекул О2 или оно связано с действием других свободных радикалов, возникающих в условиях гипероксии.
В механизме токсического действия О2 некоторые авторы существенное значение придают свободным радикалам, которые, по-видимому, образуют Н2О2 и органические перекиси, разрывающие внутримолекулярные связи ферментов, содержащих сульфгидриль-ные группы. Эта гипотеза основана на наблюдениях, которыми было установлено, с одной стороны, повышенное образование свободных радикалов в тканях животных в условиях гипероксии, а с другой — была показана возможность снижения токсического действия О2, в частности, повреждения мембраны эритроцитов посредством введения антиоксидантов (мексамина, токоферола — витамина Е и др.), ингибирующих действие свободных радикалов.
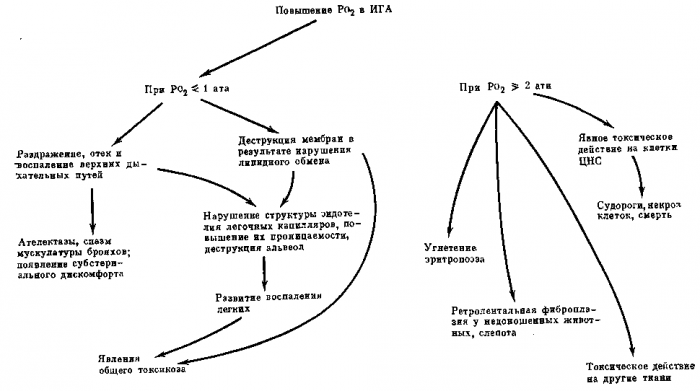
Для понимания причин возникновения симптомов токсического действия О2 важное значение имеет представление о механизме влияния гипероксии на различные функциональные системы организма. На рис. 1 представлена несколько модифицированная на основании ряда работ схема Ламбертсена, иллюстрирующая механизмы токсического действия О2 на организм животных и человека.
Исследования с участием человека, а также опыты на животных позволили установить, что токсическое действие О2 зависит от величины Р О2, от времени пребывания в условиях гипероксической среды, а также от видовой и индивидуальной чувствительности животных и человека к этому фактору.
Латентный период проявления токсического влияния О2 для различных тканей неодинаков и зависит также от величины Р О2.
В зависимости от величины Р О2 в ИГА можно условно выделить три зоны с различным проявлением токсического действия О2.
I. При Р О2 1500—2000 мм рт. ст. и выше проявляются преимущественно симптомы отравления, характерные для поражения центральной нервной системы: тошнота, головокружение, зрительные расстройства, локальные и генерализованные клонические судороги. При этом возникают патологические изменения в системе кровообращения и дыхания. Так, у животных при гипербарической гипероксии Вудом и сотр. было обнаружено резкое повышение артериального давления, по-видимому, нейрогенного происхождения; развитие сердечной недостаточности с повышением давления в сосудах малого круга, которое, вероятно, и является причиной первичного нарушения структуры легочных капилляров и последующего развития острого отека легких.
II. При Р О2 в диапазоне 760—400 мм рт. ст. токсическое действие О2 преимущественно проявляется в поражении органов дыхания: в раздражении верхних дыхательных путей, включая развитие бронхита, а затем в развитии воспаления и отека легких.
III. При Р О2 порядка 400—280 мм рт. ст. длительное пребывание в ИГА может, по-видимому, вызвать изменения как в органах дыхания, так и в системе крови и в лимфоидной ткани.
В соответствии с задачами космонавтики практическое значение для нормирования содержания О2 в ИГА имеет выяснение предельно допустимых величин Р О2, при которых еще не проявляется токсическое действие О2.
Опыты показали, что пребывание животных в среде, состоящей практически из чистого кислорода, в условиях нормального барометрического давления приводит их к гибели в результате развития воспаления легких.
Эксперименты, проведенные с белыми крысами — животными, высокочувствительными к токсическому действию О2,— позволили установить последовательность морфологических изменений, возникающих в легких в различные периоды времени нахождения их в гипероксической ИГА.
Рис. 1. Механизмы токсического действия кислорода на организм человека и животных (по Лам-бертсену, схема несколько модифицирована)
Так, при Р О2, равном 1 атм, у животных отмечали: через 1 час ателектазы; через 3—6 час. нарушения структуры капилляров и изменения их проницаемости; в течение первых суток развитие отека легких, утолщение альвеолярных мембран, расширение капилляров, диа-педезные кровотечения; через 1,5 суток выраженную гиперемию легких, очаги воспаления; через 2—2,5 суток дальнейшее развитие воспаления, приводящее к «опеченению» легких.
Большинство исследователей полагает, что развитие воспаления легких в результате ги-пероксии неизбежно приводит к развитию гипоксического состояния, завершающегося гибелью подопытных животных. Это представление оспаривают А. М. Генин и др. которые при развитии у животных тяжелого гипероксического токсикоза на фоне воспаления легких обнаружили сохранение высокого напряжения О2 в тканях головного мозга.
Появление патологических изменений в легких у крыс зависит прежде всего от величины Р О2 в ИГА. Так, у животных, экспонируемых в среде чистого кислорода, воспалительные явления в легких обнаруживаются уже на вторые-третьи сутки; при снижении содержания О2 в ИГА до 75% (Р О2 — 570 мм рт. ст.) развитие воспалительных явлений в легких отмечается только через 2— 3 недели, а при 50—60% содержании О2 в ИГА у животных не было обнаружено поражений легких, несмотря на 30-суточное пребывание их в такой среде.
Некоторые исследователи отмечали, что первичный токсический эффект при относительно небольшом повышении Р О2 в ИГА проявляется в развитии ателектазов легких. Эта точка зрения базируется в основном на результатах экспериментов, в которых крысы экспонировались при пониженном барометрическом давлении в ИГА, состоявшей почти из О2. Развитие ателектазов в такой ИГА приводило к гибели некоторых животных.
Отмечены случаи развития ателектазов и у людей, дышавших чистым кислородом. Причиной их образования является закупорка слизью мелких бронхов. Это приводит к тому, что О2 из альвеол, связанных с закупоренным бронхом, быстро диффундирует в кровь. Скорость спадения альвеол при этом зависит от химического состава заполняющих их газов. Она существенно замедляется при наличии N2 и других индифферентных газов. Дю Буа и соавт. отметили различную индивидуальную предрасположенность людей к ателектазам. Это явление они объяснили неодинаковой проходимостью воздухоносных путей у различных лиц.
Анализ результатов упомянутых исследований не дает еще оснований сделать вывод о том, что развитие ателектазов легких связано главным образом с токсическим действием О2. Основной причиной их возникновения следует считать отсутствие в альвеолах газа-наполнителя — N2 или какого-либо другого индифферентного газа. В случаях сохранения в ИГА повышенных величин Р О2 введение в ИГА даже небольшого количества биологически индифферентного газа, как показали исследования Эрнстинга, Дю Буа и др., предупреждает развитие легочных ателектазов.
В экспериментах на животных отмечено, что токсическое действие О2 может проявляться в развитии «окислительной» гемолитической анемии, которая возникает, по-видимому, в результате ускоренного разрушения эритроцитов и одновременного угнетения гемопоэза.
При морфологических исследованиях были отмечены у животных, а также у человека в условиях гипероксической ИГА изменения в красном ростке костного мозга, свидетельствующие об угнетении эритропоэза. Некоторые исследователи отмечали изменения структуры эритроцитов — появление шиповидных выпячиваний — аконтоцитоз. Это послужило основанием для заключения о том, что повреждение мембран эритроцитов, равно как и торможение эритропоэза, обусловлено токсическим действием О2. При этом было показано, что введение антиоксиданта — витамина Е — предупреждает повреждение эритроцитов. Эти данные нашли, казалось бы, определенное подтверждение и в исследованиях с людьми. В частности, у космонавтов, совершивших полет на кораблях «Джемини- IV, V и VII», было отмечено снижение в периферической крови содержания гемоглобина и эритроцитов. Несмотря на бесспорность результатов, полученных в приведенных выше исследованиях, нет еще достаточных оснований связывать развитие анемии только с токсическим действием кислорода. В определенной степени ее возникновение могло быть обусловлено и влиянием других факторов полета.
Имеются также данные о том, что токсическое действие О2 при относительно небольшом повышении Р О2 (300 мм рт. ст.) приводит к угнетению системы иммунитета, вызывая патологические изменения в лимфоидной ткани.
Важный вопрос относительно предельно допустимых концентраций О2, установления верхней границы Р О2 в ИГА для больших сроков пребывания в ней человека, а также животных изучен еще недостаточно. Здесь следует отметить работы американских исследователей, которые, прежде чем использовать в кабинах космических кораблей гипероксическую ИГА (Р О2 — 258 мм рт. ст.), провели детальное изучение ее влияния на организм животных, а в дальнейшем и человека. Результаты этих работ (в одной из которых длительность эксперимента достигала 8 месяцев) дают основание для заключения, что пребывание в ИГА с Р О2, равным 258 мм рт. ст., не вызывает глубоких патологических нарушений в организме. Однако нельзя сделать и вывод об отсутствии неблагоприятного влияния такой ИГА, так как некоторые исследователи отмечали у животных периодическое появление морфологических изменений во внутренних органах. К такому заключению приводят и эксперименты на мышах, проведенные совместно с П. М. Граменицким. После 23-дневного пребывания в ИГА с Р О2, равным 260—280 мм рт. ст., при общем давлении 720 мм рт. ст. опытные животные, видимо не отличавшиеся от контрольных, при последующем помещении их в гипербарическую среду в 4 атм с 98% содержанием в ней О2 погибали значительно быстрее контрольных. На вскрытии у них были обнаружены признаки острой гиперемии и отека легких.
Для оценки значимости изменений, возникающих при гипероксии в различных функциональных системах организма, и для создания методов повышения устойчивости к ее действию важно иметь представление о механизме токсического влияния О2 на организм, а также установить, существует ли адаптация к действию этого фактора и каковы ее проявления. Этот вопрос находится еще в начальной стадии изучения.
С целью выявления адаптационных сдвигов, возникающих при длительном пребывании животных в ИГА с повышенным Р О2, проводились эксперименты, в которых осуществлялась тренировка — систематическое помещение животных в ИГА с повышенным Р О2 с последующим длительным экспонированием этих животных в газовой среде, со
стоящей практически из чистого О2, при давлении 760 мм рт. ст. Эти эксперименты не дали достаточно четких результатов: некоторые исследователи отмечали увеличение продолжительности жизни тренированных животных, другие указывали на отсутствие достоверного эффекта или даже отмечали более острое проявление токсического действия О2 у тренированных животных.
Известно, что в механизме неспецифической адаптации к действию различных неблагоприятных факторов важную роль играет функциональное состояние надпочечников. В связи с этим для выяснения вопроса о приспособлении организма к гипероксии: в результате развития неспецифических адаптационных реакций определенное значение приобретают исследования, в которых О2 на животных с удаленными надпочечниками. Однако результаты этих исследований противоречивы. Так, при воздействии высоких давлений О2 (3 атм и выше) некоторые авторы отмечали повышенную устойчивость к гипероксии адреналэктомированных животных. В работе же других авторов, экспонировавших крыс в ИГА, имевшую Р O2, равное 690—720 мм рт. ст., была отмечена, наоборот, пониженная устойчивость адреналэктомированных животных к гипероксии. Токсические проявления, связанные с поражением легких, у оперированных животных возникали в более ранние сроки и протекали в более тяжелой форме, чем у интактных животных.
Таким образом, в отличие от гипербариче-ской гипероксии при нормобарической гипероксии механизм неспецифической адаптации играет определенную роль. По-видимому, различия в механизме токсического действия О2 при высоком его давлении и при нормальном барометрическом давлении определили и различные эффекты адреналэктомии в приведенных выше работах.
Обобщая данные литературы, можно прийти все же к выводу, что живые организмы, хотя и располагают приспособительными реакциями к нормобарической гипероксии, однако эффективность этих реакций невелика.
Первостепенное практическое значение для формирования ИГА имеют сведения о токсическом действии гипероксии на организм человека.
Решение этого важного для практики вопроса встречает определенные трудности, которые обусловлены прежде всего отсутствием точных критериев токсического действия О2, т. е. признаков, свидетельствующих о том, что дальнейшее пребывание человека в гипе-роксической среде уже сопряжено с опасностью для состояния здоровья. Значительные различия индивидуальной устойчивости человека к действию гипероксии, так же как и многочисленные факторы самого полета, оказывающие влияние на устойчивость к гипероксии, усложняют решение этой задачи.
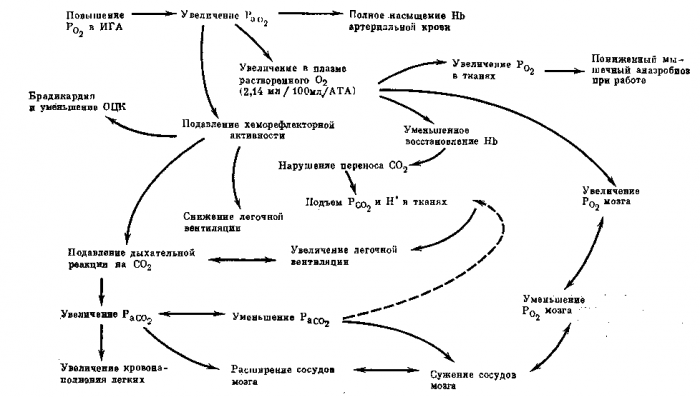
Для обоснования критериев, характеризующих раннее проявление токсического действия О2, существенное значение имеет раскрытие физиологических и патофизиологических механизмов влияния гипероксии на организм человека. Как видно из данных, приведенных на рис. 3, реакции организма в условиях гипероксии достаточно многообразны, при этом некоторые из них следует оценивать как приспособительные, так как они направлены на снижение транспорта О2 к тканям. Речь идет о снижении легочной вентиляции, частоты сердечных сокращений, уменьшении минутного объема крови, сужении сосудов мозга. Эти реакции возникают уже в первые минуты пребывания человека в гипероксической среде. Одни из них (снижение частоты сердечных сокращений, уменьшение объема циркулирующей крови) сохраняются долго, почти на протяжении всего времени пребывания человека в ИГА с повышенным Р О2, другие постепенно исчезают. Так, в начальном периоде гипероксии, когда испытуемые в условиях нормального барометрического давления дышали чистым кислородом, легочная вентиляция, по-видимому, в результате инактивации хеморецепторов синокаротидной зоны снижалась в среднем на 10%. Этот эффект сохранялся в течение некоторого времени, после чего было отмечено постепенное повышение легочной вентиляции. Это повышение обусловлено задержкой в тканях СО2, возникающей в результате снижения транспорта ее кровью. Последнее связано с падением содержания в крови восстановленного гемоглобина.
Многие авторы отмечают, что снижение жизненной емкости легких (ЖЕЛ) при гипероксии является симптомом, имеющим важное значение для ранней диагностики токсического действия О2.
Рис. 3. Физиологические сдвиги при гипероксии по Ламбертсену. (ОЦК — объем циркулирующей крови)
Снижение ЖЕЛ на 20— 30% и больше является показателем выраженного токсического действия О2, однако столь значительное снижение возникает, как правило, или непосредственно перед появлением загрудинных болей, или уже тогда, когда испытуемые жалуются на боль в груди во время глубокого вдоха, т. е. уже в период выраженного развития клинической картины кислородной интоксикации.
В связи с тем, что развитие легочной патологии является важнейшим фактором, лимитирующим время пребывания человека в условиях ИГА с повышенным Р О2, естественно, возникает мысль, что некоторые параметры газообмена и биофизические характеристики легких, такие, как диффузионная способность, растяжимость, могут быть использованы для ранней диагностики токсического действия О2.
Литературные данные относительно изменений диффузионной способности легких (DL) при гипероксии немногочисленны и противоречивы. Так, некоторые авторы не нашли изменений ее у людей, пребывавших в течение нескольких часов в среде О2 с давлением в 1 атм, и в то же время есть работы, в которых установлено снижение DL у людей в такой ИГА. Так, Эрнстинг (1961) установил снижение DL у человека уже через 3 часа после начала дыхания чистым кислородом в условиях нормального барометрического давления. При этом он отметил отчетливое уменьшение DL, указывавшее на то, что этот эффект обусловлен изменением проницаемости легочной мембраны.
М. А. Тихонов и др. также отмечали у людей в процессе 24-часового дыхания О2 при давлении 1 атм прогрессирующее снижение DL начиная с 8-го часа. В некоторых случаях к концу исследования через 24 часа снижение DL достигало 12%. Однако при этом не было установлено достоверной корреляции данного показателя с клинической картиной проявления токсического действия О2. В этой же работе было отмечено снижение растяжимости легких, в среднем на 16%. Растяжимость легких является интегральным показателем, который зависит как от собственно эластических свойств легочной паренхимы, так и от состояния кровенаполнения легких' и сил поверхностного натяжения жидкостной пленки, выстилающей альвеолы. По-видимому, снижение растяжимости легких, равно как уменьшение ЖЕЛ при гипероксии, связано с развитием ателектазов, а также, возможно, с увеличением кровенаполнения легких. Из сказанного можно сделать заключение, что изменения DL растяжимости легких могут иметь определенное значение для суждения о токсическом действии О2, но практически эти показатели использовать достаточно трудно.
Клинические проявления токсического действия О2 — кашель, сухость во рту, болевые
или неприятные ощущения в загрудинной области — являются наиболее постоянными признаками, указывающими на развитие выраженной кислородной интоксикации. Появление этих признаков, особенно загрудинных болей, как правило, являлось сигналом для прекращения исследований. Это обусловлено тем, что загрудинные боли после их возникновения, как правило, неуклонно нарастают и сопровождаются болями в межреберных мышцах, появлением одышки и ухудшением
общего состояния обследуемого. Механизм возникновения загрудинных болей и субстернального дискомфорта связан с возникновением ателектазов, а также, возможно, с развитием спазма бронхов. Определенную роль при этом, вероятно, играет развитие отека слизистой оболочки бронхов.
Возникновению загрудинных болей часто предшествует появление признаков раздражения верхних дыхательных путей: сухость во рту, першение в носоглотке, кашель. Через 6—12 час. после прекращения исследования — выхода из гипероксической среды — эти явления, как и жалобы на загрудинные боли, полностью исчезают. Однако на симптомы раздражения верхних дыхательных путей следует обращать серьезное внимание, так как известны случаи, когда их появление предшествовало развитию острого трахео-бронхита и воспаления легких.
В исследованиях с участием людей, даже при значительном повышении Р О2 в ИГА (до 1 атм), были обнаружены существенные индивидуальные различия чувствительности к токсическому действию О2.
В работе А. М. Генина и др. было отмечено, что при дыхании кислородом (1 атм) в течение 24 час. появление клинических симптомов токсического действия О2 отмечается не у всех испытуемых и в различные промежутки времени. На рис. 4 приведены данные, характеризующие частоту и время появления симптомов раздражения верхних дыхательных путей и загрудинных болей в этих исследованиях.
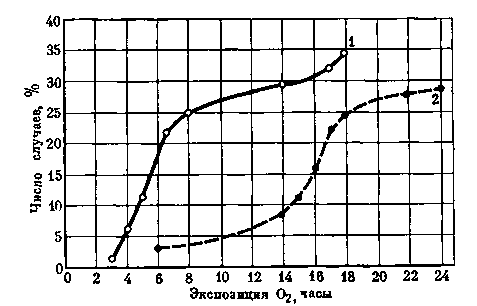
Рис. 4. Динамика развития различных симптомов токсического действия кислорода у людей при 24-часовом дыхании кислородом (по Генину и Тихонову и др.)
1 — жалобы на сухость, першение в горле, появление
кашля;
2 — жалобы на появление неприятных и болевых ощу
щений в области груди.
Число случаев появления жалоб в процентах от количества испытуемых представлено нарастающим итогом
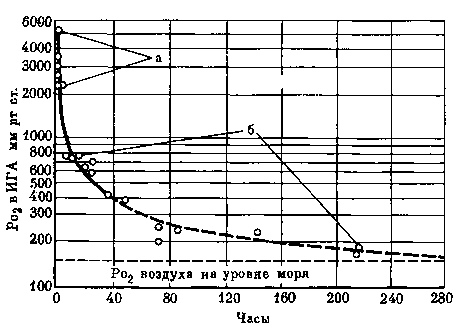
Рис. 5. Время появления различных симптомов токсического действия кислорода в зависимости от величины Р О2 в ИГА (составлен доктором Ротом по данным Велча и сотр.; Моргана и сотр.)
а — грубые расстройства ЦНС, судороги; б — першение в горле, кашель, загрудинные боли
Значительные индивидуальные различия в проявлении токсического действия О2, вероятно, являются причиной расхождения литературных данных о границе проявления токсического действия О2. Так, например, А. М. Генин, С. Г. Жаров и др. не обнаружили признаков токсического действия О2 при 30-дневном пребывании испытуемых в ИГА с Р О2, равным 290—280 мм рт. ст., в то время как Велч отмечал развитие токсического действия О2 при меньших сроках пребывания в ИГА с меньшей величиной Р О2 (200 мм рт. ст.). Столь значительные различия индивидуальной чувствительности людей к гипероксии создают большую трудность в определении предельно допустимого содержания О2 в ИГА кабин при длительных полетах.
Время проявления токсического действия 02 зависит от величины Р О2 в ИГА и сокращается по мере его увеличения. Это отчетливо видно на рис. 5, где представлены данные о времени и характере проявления токсического действия О2 при различных величинах Р О2 в ИГА. При оценке данных, представленных на этом рисунке, обращает на себя внимание то, что пребывание в течение 220 час. в ИГА даже с незначительно повышенным Р О2 (200 мм рт. ст.), как показали исследования Велча и др., может приводить к развитию у некоторых людей симптомов токсического действия кислорода. В связи с тем, что отдельные люди обладают весьма высокой чувствительностью к токсическому действию О2, вряд ли можно рассчитывать в длительных полетах (многомесячных) на использование ИГА с Р О2, существенно превышающим его величину в атмосферном воздухе. Вопрос о том, какие причины определяют столь различную индивидуальную чувствительность людей к гипероксии, изучен еще недостаточно, в связи с чем нет надежных критериев для отбора высокочувствительных лиц и нет средств, заметно повышающих их устойчивость к этому фактору.
Из сказанного можно сделать заключение, что верхняя граница величины Р О2 в ИГА применительно к длительным (многомесячным) полетам еще не определена, однако ознакомление с историей изучения токсического действия О2 на организм человека позволяет сделать вывод о том, что граница токсического действия неуклонно снижается и в настоящее время она лишь предположительно может быть определена в диапазоне таких величин Р О2 в ИГА, при которых РА О2 возрастает примерно до 150—200 мм рт. ст.
В связи со сказанным можно понять причину, по которой американские специалисты решили отказаться в полетах на «Скайлэ-бе» от моногазовой гипероксической ИГА (Р О2=258 мм рт. ст.).
При обсуждении вопроса о верхней границе Р О2 в ИГА следует отметить, что для точного установления ее необходимо получение дополнительной информации. Речь идет о том, что до сих пор нет данных о том, как влияют на устойчивость к гипероксии выполнение физической работы, повышение и понижение температуры окружающей среды и многие другие факторы, которые могут иметь место в полетах.
В случаях же необходимости осуществления полетов в зонах с высокой радиацией, наличие в ИГА повышенного уровня Р О2, вероятно, окажется нежелательным. Такое заключение можно сделать на основании многочисленных экспериментальных исследований, в которых была установлена повышенная чувствительность к ионизирующему излучению животных во время пребывания их в гипероксической ИГА. При этом причину упомянутого эффекта принято объяснять определенным сходством механизмов токсического действия на ткани О2 и ионизирующего излучения.
До сих пор не обсуждается вопрос и о том, может ли оказать влияние на чувствительность организма к повышенному содержанию О2 в ИГА такой важный фактор полета, как невесомость. В то же время есть определенные основания считать, что невесомость, равно как и выполнение физической работы, а также температурные воздействия, по-видимому, могут приводить к некоторому повышению чувствительности организма к гипероксии. Такое предположение основано на том, что одной из адаптационных реакций организма при гипероксии является сужение сосудов мозга, сердца и легких, определяющее уменьшение транспорта кислорода к тканям этих органов. В условиях невесомости происходит перераспределение кровотока, увеличение кровонаполнения областей тела, лежащих выше сердца, в связи с чем упомянутые выше адаптивные сосудистые реакции, вероятно, уже не смогут достаточно полно проявиться.
Вместе с человеком в длительных полетах, очевидно, будут находиться растения и различные виды животных, которые могут оказаться высокочувствительными к действию гипероксии. В связи с этим целесообразно получить информацию о токсическом влиянии О2 на представителей растительного и животного мира, планируемых для использования в полетах.
Скачать реферат:
Пароль на архив: privetstudent.com