Зарождение кристаллов
Наибольшее число экспериментальных работ по зарождению кристаллов принадлежит Г. Тамману.
Особо интересны его исследования способности кристаллизации вещества, которую он определяет почти постоянным числом центров кристаллизации, возникающим в единицу времени в единице объема при некоторой температуре переохлажденной жидкости.
Определение способности кристаллизации производилось следующим образом.
Небольшое количество исследуемого органического вещества расплавлялось и быстро охлаждалось до температуры экспозиции, при которой вещество выдерживалось определенное время, необходимое для образования центров кристаллизации. После этого вещество выращивалось при более высокой температуре, близкой к температуре плавления. При этих условиях новые центры уже не могли образовываться. На рис. 12 по оси абсцисс откладывается переохлаждение, т. е. разность между температурой плавления (Тпл) и температурой экспозиции (Тэк), а по оси ординат — число центров кристаллизации (ЧЦ) в определенном объеме. При температуре плавления (0) число зарождающихся центров кристаллизации равно нулю. По мере увеличения переохлаждения ЧЦ растет, достигая максимума при определенном переохлаждении, и далее вновь уменьшается до нуля (А). Точка А соответствует переохлаждению, при котором вещество уже не способно к самопроизвольной кристаллизации и при дальнейшем охлаждении застывает в стеклообразную, аморфную массу.
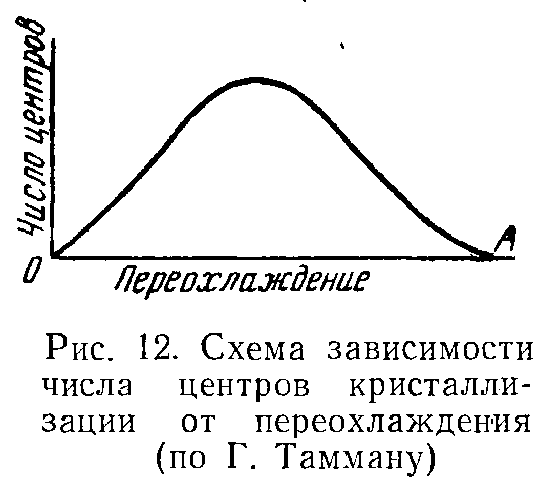
Сейчас всеми признается ошибка Таммана в истолковании этих по существу правильных экспериментов. Исследованные им органические вещества не очищались от посторонних взвешенных в них твердых частиц, и Тамман наблюдал не спонтанную кристаллизацию, а кристаллизацию на этих частицах, служивших зародышами. Известно, что наличие границы раздела двух фаз в системе облегчает процесс фазового перехода вещества. Работы Таммана, однако, представляют большой интерес, так как на практике почти всегда имеют дело с веществами, в которых присутствуют примеси.
По своей природе поверхность раздела двух фаз (затравка), на которой осуществляется кристаллизация, может быть разнообразной:
1) наиболее эффективна твердая кристаллическая пылинка растворенного вещества;
2) хорошей затравкой может быть частица такого вещества, которое способно давать с растворенным веществом твердый раствор; например, для алюмо-калиевых квасцов затравкой служит кристаллит хромовых квасцов;
3) затравкой может служить кристаллик такого вещества, которое может давать с растворенным веществом закономерные сростки или структура которого близка к структуре растворенного вещества;
4) затравкой оказываются многие частицы, которые способны на своей поверхности адсорбировать молекулы растворенного вещества.
Однако затравка должна иметь не только определенное строение или определенные свойства поверхности, но ее размеры должны быть выше некоторой границы. Частицы, достигшие критического размера и большего, чем критический, будут зародышами кристаллизации. Частицы, не достигшие критического размера, остаются термодинамически неустойчивыми; в результате тепловых флуктуаций они возвращаются в жидкую фазу. Критический размер зародыша тем меньше, чем больше скрытая теплота кристаллизации и степень (переохлаждения и чем меньше его удельная поверхностная энергия:
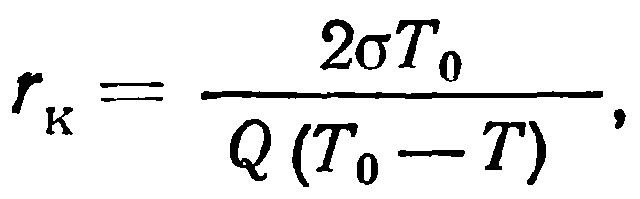
где rк — критический размер зародыша, а — поверхностная энергия, Q — скрытая теплота кристаллизации, (Tо—Т) — степень переохлаждения системы.
Частицы кристаллов некоторых веществ, достигшие примерно десятых долей микрона, уже могут оказаться способными «заразить» раствор (расплав), находящийся в метастабильном состоянии.
1. Решающим фактором в зарождении кристаллов остается переохлаждение. Чтобы обеспечить переохлаждение, необходимо устранить из системы всякие твердые частицы. Это достигается путем предварительного нагрева жидкости значительно выше температуры плавления, ее тщательной фильтрации и защиты жидкости от пылинок извне.
Опытами В. И. Данилова показано, что зависимость переохлаждения жидкости от ее перегрева определяется наличием в ней нерастворимых примесей. Нагреванием жидкости до определенной температуры выше точки кристаллизации примеси могут быть дезактивированы. В частности, при предварительном нагревании жидкого олова до 80—90° С выше точки кристаллизации, достигались максимальные переохлаждения. Полная дезактивация примесей в висмуте происходит при перегреве на 40—50° С.
Для получения переохлажденных жидкостей, как следует из кривой, полученной Тамманом (см. рис. 12), нужна большая скорость переохлаждения.
Опыт показывает, что способность к переохлаждению жидкостей, содержащих ионы, возрастает при увеличении заряда ионов и при уменьшении их радиусов. Присутствие ОН-группы в органических веществах способствуют переохлаждению.
2. На зарождение кристаллов оказывают влияние соприкасающиеся с жидкостью поверхности твердых тел, в частности, стенки сосуда. Отдельные участки неоднородной поверхности обладают различной активностью по отношению к образованию новой фазы. Эта активность определяется как физико-химической природой участка, так и (геометрической его формой и величиной. Такие дефекты на поверхностях твердых тел, как трещины и каналы почти молекулярного размера, способствуют зарождению кристаллов.
3. Велика роль ионизирующего излучения, например, у-излучения радия. Его эффект сводится к увеличению числа центров кристаллизации. За счет поляризующего действия возникших ионов на нейтральные молекулы первые становятся центрами окружения как ионов противоположного знака, так и этих молекул, и вокруг образующейся достаточно устойчивой системы начинается рост кристаллов.
4. Электрическое и магнитное поля также способствуют зарождению кристаллов. При этом возникающее число центров кристаллизации находится в прямой зависимости от напряженности поля. В электрическом или магнитном поле молекулы вещества (переохлажденной жидкости), ориентируясь в одном направлении, образуют анизотропную среду, во многом аналогичную кристаллической.
К изучению влияния электрического поля на зарождение кристаллов повторно возвращаются многие исследователи. М. И. Козловским установлено, что v — скорость появления новых центров кристаллизации на единицу площади при некоторой температуре прямо пропорциональна пересыщению раствора и квадрату напряженности электрического поля, но, конечно, различается для того или иного кристаллизуемого вещества
![]()
где r — коэффициент пропорциональности, (с—с0) —пересыщение, Е — напряженность поля.
5. Влияние ультразвука на процесс кристаллизации металлов впервые отметил С. Я. Соколов. Ультразвуковое поле настолько ускоряет процесс кристаллизации, что в результате получаются слитки с дендритной структурой. Механизм действия ультразвука в ультразвуковом поле сводится к происходящему на границе раздела двух фаз отщеплению мельчайших кристаллов, совершающих колебательные движения и увеличивающихся в размерах. Срастаясь с кристаллом, они образуют поликристаллический слиток. Скорость этого процесса зависит от интенсивности ультразвукового поля.