ДИПЛОМНАЯ РАБОТА
Синтез композитных регулярных систем «пористый оксид алюминия - металлические наночастицы» и их исследование фотофизическими методами и методами АСМ
Аннотация
В данной работе предложен синтез композитных регулярных систем «пористый оксид алюминия – металлические наночастицы» и их исследование фотофизическими методами и методами АСМ.
Работа состоит из введения, трёх глав и заключения.
В первой главе рассмотрены композитные наносистемы и их области применения. Также рассмотрено образование пористых оксидных структур на поверхности алюминия в процессе его анодирования и заполнение этих нанопор металлом.
Во второй главе описаны приборы и техника эксперимента.
В третьей главе приведены результаты исследований полученных образцов анодированного алюминия методами атомно-силовой микроскопии и спектральными методами. Выявлены параметры электрохимического осаждения металла, технология получения медных наночастиц и метод экспресс-контроля наноструктурированных медных частиц.
В заключительной части сформулированы основные результаты и выводы и приведен список использованных источников.
Дипломная работа содержит 65 страниц, в том числе 23 рисунка, 1 таблицу, 40 источника литературы. Графическая часть работы выполнена в виде презентаций средствами Microsoft Power Point.
The Abstract
This paper presents a synthesis of composite regular systems "porous aluminum oxide - metal nanoparticles" and their photophysical study of methods and techniques AFM.
The work consists of an introduction, three chapters and a conclusion.In the first chapter the composite nanosystems and their application. Also, consider the formation of the porous oxide structures on aluminum in the process of anodizing and filling these nanopores metal.
The second chapter describes the instruments and experiment.The third chapter presents the results of the analyzes of these samples anodized aluminum by atomic force microscopy and spectroscopic methods. Identified parameters of the electrochemical precipitation of metal technology of copper nanoparticles and the method of express-control of nanostructured copper particles.
In the final part of the state the main results of water-and you and a list of sources used. Diploma thesis contains 65 pages, including 23 figures, 1 table, 40 sources of literature. Graphic part of the work was done in the form of presentations by means of Microsoft Power Point.
Содержание
Введение…………………………………………………………………………..7
1 Композитные наноструктуры………………………………………………….9
1.1 Квантовые ямы………………………………………………………………..9
1.2 Квантовые проволоки……………………………………………………….16
1.3 Квантовые точки…………………………………………………………….18
1.4 Фуллерены……………………………………………………………………20
1.5 Эндометаллфуллерены………………………………………………………23
1.6 Пористый оксид алюминия…………………………………………………29
1.7 Факторы, влияющие на рост анодной окисной пленки на алюминии………………………………………………………………………………..34
1.8 Заполнение пор металлом…………………………………………………..38
2 Приборы и техника эксперимента…………………………………………...42
2.1 Электролитическая ванна…………………………………………………..42
2.2 Используемые растворы и образцы………………………………………..44
2.3 Измерения на атомно-силовом микроскопе……………………………….45
2.4 Подготовка образцов………………………………………………………..46
3 Экспериментальная апробация технологии синтеза композитных наноструктур «пористый окид - металл»………………………………………………49
3.1 Получение пористого оксида……………………………………………….49
3.2 Электрохимическое осаждения металла…………………………………...51
3.3 Перспективные наносистемы, получаемые на основе пористого оксида заполненного металлом…………………………………………………………54
Заключение………………………………………………………………………62
Список используемых источников…………………………………..…………63
Введение
В последние годы одним из приоритетных научных направлений в России является исследование наносистем и развитие нанотехнологий. Наносистемы представляют практический и научный интерес как для понимания фундаментальных электронных, магнитных, оптических, тепловых и механических свойств материалов, имеющих нанометровые размеры, так и с точки зрения создания на их основе приборов с принципиально новыми физическими свойствами, обеспечивающих существенное повышение функциональных характеристик электронных и оптических приборов, а также сенсоров [1,2].
На возможность роста окисных пленок на алюминиевом аноде и на техническую применимость подобных покрытии впервые указал наш соотечественник — казанский химик Н. II. Слугинов в 1878 г. В дальнейшем число научных работ, посвященных исследованию анодного окисления алюминия, сильно возросло.[3] Такой большой научный интерес к явлениям анодного окисления алюминия объясняется большим практическим значением этого процесса для получения защитных покрытий на поверхности деталей из алюминия [4].
Несмотря на широкое использование и повышенный интерес к электролитическому оксидированию, механизм этих процессов изучен недостаточно. Многообразие воззрений на механизм и кинетику протекающих реакций затрудняет эффективное решение технологических задач. Таким образом, тема работы актуальна.
Анодные оксидные пленки нашли широкое применение в различных областях науки и техники, например, для формирования наноразмерных структур в электронных, магнитных и фотонных приборах [1,3] и поэтому являются предметом интенсивного изучения [4,5,6]. Комбинация уникальной пористой структуры (прямые поры управляемого диаметра) с высокой температурной, механической и химической стабильностью делает пленки анодированного оксида алюминия привлекательным материалом для различных применений в области фильтрации и разделения смесей, хранения информации, в сенсорике и для синтеза одномерных наноструктур. Мембраны анодированного оксида алюминия обладают однородной пористой структурой с гексагональной упаковкой цилиндрических каналов и узким распределением пор по размерам. Использование различных электролитов, напряжений и времен анодирования позволяет варьировать диаметр пор, расстояние между порами и толщину пленки в широких пределах.
На основе анодированного оксида алюминия возможна разработка технологии сравнительно простого получения новых типов композитных наноструктур и метаматериалов. С подобными системами связываются большие надежды в области наноэлектроники и нанотехнологий.
В данной работе нами предложена технология получения пористого оксида алюминия с контролируемым заполнением пор металлическими наночастицами на приборной и лабораторной базе ЦЛИБФ.
Для этого были сформулированы и решены следующие задачи:
1 Усовершенствовать электролитическую ванну для анодирования алюминия с плоским свинцовым электродом и подложкой для вертикального анодирования.
2 Разработать технологию заполнения нанопор оксидной матрицы анодированного алюминия металлическими наночастицами.
3 Исследовать полученные образцы анодированного алюминия методами атомно-силовой микроскопии, а также спектральными методами.
4 Предложить метод экспресс-контроля наноструктурированных медных поверхностей.
1 Композитные наноструктуры
Бурное развитие микроэлектроники и информационных технологий, в последние десятилетия, обусловлено во многом минитюаризацией элементной базы. В связи с этим огромный интерес представляют наноразмерные системы, составленные из нескольких компонентов: «полупроводник – диэлектрик», «полупроводник – металл», «металл – диэлектрик». В некоторых работах за такими системами закрепилось название композитные.
Наиболее изученными в этом ряду являются композитные системы «полупроводник – диэлектрик», «полупроводник – полупроводник», именуемые квантовыми нитями, квантовыми точками и квантовыми ямами. Остановимся более подробно на каждой из композитных наносистем.[7]
1.1 Квантовые ямы
Простейшая квантовая структура, в которой движение электрона ограничено в одном направлении, – это тонкая пленка или просто достаточно тонкий слой полупроводника. Именно на тонких пленках полуметалла висмута и полупроводника InSb впервые наблюдались эффекты размерного квантования [1]. В настоящее время квантовые структуры изготавливают иначе. Рассмотрим структуру энергетического спектра полупроводников. Этот спектр состоит из разрешенных и запрещенных энергетических зон, которые сформированы из дискретных уровней атомов, образующих кристалл. Самая высокая энергетическая зона называется зоной проводимости. Ниже зоны проводимости расположена валентная зона, а между ними лежит запрещенная зона энергий. У одних полупроводников запрещенные зоны широкие, а у других более узкие. Что произойдет, если привести в контакт два полупроводника с различными запрещенными зонами (граница таких полупроводников называется гетероструктурой). На рисунке 1 изображена граница узкозонного и широкозонного полупроводников. Для электронов, движущихся в узкозонном полупроводнике и имеющих энергию меньше , граница будет играть роль потенциального барьера. Два гетероперехода ограничивают движение электрона с двух сторон и образуют потенциальную яму.
Таким способом и создают квантовые ямы, помещая тонкий слой полупроводника с узкой запрещенной зоной между двумя слоями материала с более широкой запрещенной зоной. В результате электрон оказывается запертым в одном направлении, что и приводит к квантованию энергии поперечного движения. В то же время в двух других направлениях движение электронов будет свободным, поэтому можно сказать, что электронный газ в квантовой яме становится двумерным. Таким же образом можно приготовить и структуру, содержащую квантовый барьер, для чего следует поместить тонкий слой полупроводника с широкой запрещенной зоной между двумя полупроводниками с узкой запрещенной зоной.
Рисунок 1 – Энергетические зоны на границе двух полупроводников - гетероструктуре. и - границы зоны проводимости и валентной зоны, Eg - ширина запрещенной зоны. Электрон с энергией меньше (уровень показан красным цветом) может находиться только справа от границы
Когда движение электрона происходит в ограниченной области, его энергия имеет строго определенные, дискретные значения. Говорят, что спектр энергий квантован.
В квантовой механике электрон не бегает в ограниченной области, как классическая частица. Если он заперт в атоме, молекуле или любой потенциальной яме, то волновая функция Ч представляет стоячую волну. Если речь идет о прямоугольной потенциальной яме, которая изображена на рис. 2, то по своей форме волна будет такой же, как и в случае натянутой струны, но дискретным в этом случае будет не спектр частот, а спектр энергий. Стоячие волны, описывающие электронные состояния в яме, – это синусоиды, обращающиеся в точках x = 0 и x = a в нуль.
Рисунок 2 – Волновые функции и уровни энергии частицы, находящейся в бесконечно глубокой потенциальной яме
Показаны три нижних энергетических уровня (красный цвет) и три волновые функции
, (1)
где n– номер квантового состояния;
a – размер ямы.
На рисунке 2 изображены три такие функции, соответствующие n = 1, 2, 3, … Электронная плотность в яме распределяется неравномерно, есть максимумы и минимумы плотности вероятности. Из формулы (1) следует также, что длины волн Ч'-функций, описывающих электронные состояния с различными n, удовлетворяют условиям , то есть в яме укладывается целое число полуволн.
Особенности энергетических уровней
Найдем разрешенные уровни энергии электрона, находящегося в потенциальной яме. Воспользуемся правилом квантования Н. Бора.[8] Согласно постулату Бора, в потенциальной яме разрешены лишь те траектории, для которых импульс частицы и ширина ямы связаны соотношением
(2)
где n – номер квантового состояния. Определив отсюда разрешенные значения импульса, найдем и уровни энергии в яме:
(3)
Минимальная энергия частицы, находящейся в яме, не может быть равной нулю. Всегда существует так называемая энергия нулевых колебаний, которая, согласно формуле 3, равна n2h2 . Вычислим, какой порядок имеет величина первого уровня в реальной квантовой яме. Если ширина ямы равна 5 нм, то, согласно (3), имеем E1 = 0,02 эВ. Нужно, однако, иметь в виду, что электронная масса в кристалле может существенно отличаться от массы свободного электрона m = 10-27 г. В типичной ситуации эффективная масса в квантовой яме в десять раз меньше массы свободного электрона. Тогда при той же ширине ямы получим E1 = 0,2 эВ. Эта величина и определяет характерный масштаб электронных энергий в квантовых структурах.
Применение квантовых наноструктур в электронике
Рассмотрим принцип действия двух основных приборов современной квантовой электроники.
Резонансный туннельный диод
В классической физике если полная энергия частицы меньше потенциальной энергии в области барьера, то эта частица отражается и затем движется в обратном направлении. В том случае, когда полная энергия превышает потенциальную, барьер будет преодолен. Квантовая частица ведет себя иначе: она преодолевает барьер подобно волне. Даже если полная энергия меньше потенциальной, есть вероятность преодолеть барьер. Это квантовое явление получило название "туннельный эффект". Оно используется в резонансном туннельном диоде.
Он состоит из двух барьеров, разделенных областью с малой потенциальной энергией. Область между барьерами – это как бы потенциальная яма, в которой есть один или несколько дискретных уровней. Характерная ширина барьеров и расстояние между ними составляют несколько нанометров. Области слева и справа от двойного барьера играют роль резервуаров электронов проводимости, к которым примыкают контакты. Электроны занимают здесь довольно узкий энергетический интервал. В приборе используется следующая особенность двойного барьера: его туннельная прозрачность имеет ярко выраженный резонансный характер. В том случае, когда энергия электронов, налетающих на барьеры, равна энергии дискретного уровня, туннельная прозрачность резко возрастает.[9] При резонансе из-за интерференции волн во внутренней области гасится волна, отражающаяся от двойного барьера. Следовательно, волна, упавшая слева, полностью проходит направо.
Рассмотрим, как работает резонансный диод. Ток, протекающий через двойной барьер, зависит от величины приложенного напряжения. Потенциал в приборе падает главным образом в области двойного барьера, так как области слева и справа от него обладают высокой проводимостью. Если приложенное напряжение мало и энергия электронов, налетающих на барьер слева, меньше энергии дискретного уровня, то прозрачность барьера и, следовательно, протекающий ток будут малы. Ток достигает максимального значения при таких напряжениях, когда энергия электронов равна энергии дискретного уровня. При более высоких напряжениях энергия налетающих электронов станет больше энергии дискретного уровня и туннельная прозрачность барьера уменьшится. При этом ток также уменьшится. На вольт-амперной характеристике будет участок отрицательного дифференциального сопротивления. Благодаря этому в электронных схемах резонансный диод может использоваться не только как выпрямитель, но и выполнять самые разнообразные функции. Если к центральной области резонансного диода подвести контакт, через который можно управлять положением дискретного уровня, получится новый прибор – транзистор.
Лазеры на квантовых ямах
Квантовые структуры используются для создания лазеров. Уже сегодня эффективные лазерные устройства на квантовых ямах дошли до рынка и применяются в волоконно-оптических линиях связи. Для работы любого лазера необходимо создать инверсную населенность энергетических уровней. То есть, на более высоком уровне должно находиться больше электронов, чем на низком, в то время как в состоянии теплового равновесия ситуация обратная. Каждому лазеру необходим оптический резонатор или система зеркал, которая запирает электромагнитное излучение в рабочем объеме.
Для того чтобы квантовую яму превратить в лазер, нужно ее подсоединить к двум контактам, через которые электроны могут непрерывно поступать в рабочую область. Пусть через один контакт электроны поступают в зону проводимости. Далее, совершая скачки из зоны проводимости в валентную зону, они будут излучать кванты, то есть порции электромагнитного излучения, схема которого представлена на рисунке 3. Затем через валентную зону носители тока должны уходить на другой контакт.
Рисунок 3 – Энергетическая схема лазера на квантовой яме другой контакт
Частота излучения w определяется условием
, (4)
где и – энергии первых энергетических уровней соответственно в зоне проводимости и валентной зоне;
– ширина запрещенной зоны.
Электромагнитное излучение, генерируемое лазером, нужно сконцентрировать в центральной, рабочей области прибора.[10] Для этого показатель преломления внутренних слоев должен быть больше, чем внешних. Внутренняя область играет роль волновода. На границах этого волновода нанесены зеркала, которые образуют резонатор.
Лазеры на квантовых ямах обладают преимуществами по сравнению с обычными полупроводниковыми лазерами. Эти приборы можно перестраивать, управляя параметрами энергетического спектра. Так, при уменьшении размеров ямы минимальные энергии электронов в зоне проводимости и в валентной зоне увеличиваются и, согласно формулам (3) и (4), частота, генерируемая лазером, возрастает. Подбирая толщину квантовой ямы, можно добиться, чтобы затухание волны в оптической линии связи, в которую поступает излучение,[11] было минимальным. Лазеры на квантовых структурах очень экономны, они питаются меньшим током, чем другие полупроводниковые лазеры, и дают больше света на единицу потребляемой энергии – до 60% электрической мощности преобразуется в свет.
- Квантовые проволоки
Квантовыми проволоками называют структуры толщиной всего в один атом. Специалисты из исследовательского центра IBM Н.Д. Ланг и П. Авурис выполнили теоретический расчет проводимости квантовой проволоки, состоящей из атомов углерода. Согласно их вычислениям, проводимость квантовой проволоки при увеличении ее длины изменяется не монотонно, а колеблется. Она достигает максимумов для проволоки, состоящей из четного числа атомов, поскольку в этом случае больше число допустимых электронных состояний.[12] В Японии. Х. Ониши и его коллеги из Токио создали квантовую проволоку из атомов золота между иглой сканирующего туннельного микроскопа и поверхностью золотого образца. При увеличении расстояния между иглой и поверхностью проволока становится длиннее и тоньше. Проводимость проволоки при ее растяжении изменялась скачками на квантовую единицу проводимости . Такое же скачкообразное изменение проводимости наблюдалось и в университете Лейдена (Нидерланды). Созданная там квантовая проволока представляла собой микроскопический мост между двумя концами надломленной золотой проволоки.
Одним из наиболее важных следствий получения одномерных баллистических каналов внутри гетероструктур GaAs-AGaAs и кремниевых сверхрешёток стало обнаружение квантования проводимости в зависимости от напряжения на затворе, управляющего шириной квантовой проволоки, которое проявляется в виде серии плато одномерной проводимости, разделенных ступенями величиной ; где и – спиновый и долинный факторы соответственно. Рост напряжения на затворе приводит к увеличению ширины квантовой проволоки, тем самым стимулируя заполнение большего числа подзон размерного квантования. При этом зависимость G(Vg) имеет ярко выраженный ступенчатый характер, так как кондактанс квантовой проволоки изменяется скачком каждый раз, когда уровень Ферми совпадает с одной из подзон размерного квантования:
, (6)
где N-число заполненных подзон размерного квантования, которое соответствует номеру верхней заполненной одномерной подзоны квантовый проволоки.
Рисунок 4 – Схема расщепленного затвора (при напряжении Ug), используемая для получения модулированных квантовых проволок внутри квантовых ям
Наблюдаемая величина ступенек квантованной проводимости, как правило, несколько меньше, чем что наглядно показывает нам рисунок 4 (б), это может быть результатом влияния спиновой поляризации носителей в нулевом магнитном поле [13] или нарушение когерентности по причине как электрон-электронного взаимодействия, так и рассеяния на примесных центрах. Остаточные примеси, распределенные вдоль границ квантовой проволоки, являются основой при создании внутренних барьеров, которые модулируют характеристики одномерного транспорта. Мощность подобных барьеров регулируется путем изменения напряжения на затворе, управляющего шириной квантовой проволоки, и особенно-с помощью дополнительных “пальчиковых” затворов, применяемых для применения квантовых точек между двумя соседними барьерами, как видно из рисунка 4 (а).
Напряжение и прикладываются к “пальчиковым” затворам, предназначенным для реализации квантовых точек; б-Квантованная проводимость G(Ug),обнаруженная при T=77 K для узкого одномерного [14] канала (2*2нм2) в самоупорядоченной кремниевой квантовой яме p-типа. Положение уровня Ферми соответствует заполнению одномерных подзон тяжелых дырок .
1.3 Квантовые точки
Технологи разработали несколько способов получения квантовых точек. Эту структуру можно сформировать также как и квантовые нити, на границе раздела двух полупроводников, где находится двумерный электронный газ, или нанести дополнительные барьеры, ограничивающие движение электронов еще в одном или двух направлениях.
На рисунке 5 показаны квантовые точки, созданные на границе раздела арсенида галлия и арсенида алюминия–галлия. В процессе роста в полупроводник AlGaAs были введены дополнительные примесные атомы. Электроны с этих атомов уходят в полупроводник GaAs, то есть в область с меньшей энергией. Но они не могут уйти слишком далеко, так как притягиваются к покинутым ими атомам [15] примеси, получившим положительный заряд. Практически все электроны сосредоточиваются у самой гетерограницы со стороны GaAs и образуют двумерный газ. Процесс формирования квантовых точек начинается с нанесения на поверхность AlGaAs ряда масок, каждая из которых имеет форму круга. После этого производится глубокое травление, при котором удаляется весь слой AlGaAs и частично слой GaAs.
Рисунок 5 – Квантовые точки, сформированные в двумерном электронном газе на границе двух полупроводников
В результате электроны оказываются запертыми в образовавшихся цилиндрах (область, где находятся электроны, окрашена в красный цвет). Диаметры цилиндров имеют порядок 500 нм.
Особенность квантовых точек
В квантовой точке движение ограничено в трех направлениях и энергетический спектр полностью дискретный, как в атоме. Поэтому квантовые точки называют еще искусственными атомами, хотя каждая такая точка состоит из тысяч или даже сотен тысяч настоящих атомов. Размеры квантовых точек (можно говорить также о квантовых ящиках) порядка нескольких нанометров. Подобно настоящему атому, квантовая точка может содержать один или несколько [16] свободных электронов. Если один электрон, то это как бы искусственный атом водорода, если два – атом гелия и т.д.
Кроме простого нанесения рисунка на поверхность полупроводника и травления для создания квантовых точек можно использовать естественное свойство материала образовывать маленькие островки в процессе роста. Такие островки могут, например, самопроизвольно образоваться на поверхности растущего кристаллического слоя.
В последнее время во многих лабораториях мира ведутся работы по созданию лазеров на квантовых точках.
Ещё одним активно изучаемым типом наноструктур являются фуллерены и их композитный вариант эндометаллфуллерены.
- Фуллерены
Фуллерены были открыты в 1985 г. Это аллотропные формы углерода, которые содержат чётное (более 20) количество атомов углерода, образующих три связи друг с другом. Атомы в молекулах фуллеренов расположены на поверхности сферы или сфероида в вершинах гексагонов и пентагонов (см рис.). Фуллерены с количеством атомов более 70 называются высшими фуллеренами. Интерес к исследованиям фуллеренов обусловлен разнообразием новых физико-химических явлений, происходящих при участии фуллеренов, и перспективами применения нового класса материалов, создаваемых на их основе.
Молекула C60 обладает наиболее высокой среди фуллеренов симметрией и наибольшей стабильностью. Каждый атом углерода в молекуле расположен в вершинах двух гексагонов и одного пентагона [2]. Валентные электроны каждого атома находятся в sp2-гибридизованных состояниях, сходных с состояниями электронов в графите. Молекулы фуллеренов являются сильными окислителями, так как атомы углерода в них обладают высокой электроотрицательностью и способны присоединять к себе до шести свободных электронов. В перспективе фуллерены могут быть применены как наноструктурные материалы. Одним из типов таких материалов являются металл-фуллереновые плёнки, осаждаемые в вакууме. Уже при малых концентрациях фуллеренов в плёнках титан-фуллерен структурообразующие частицы имеют округлую форму и размеры 15-40 нм, поэтому добавление фуллеренов в сплавы может служить способом создания нано-материалов. Еще одним особым свойством некоторых фуллерен-содержащих структур является сверхпроводимость: фуллериды щелочных металлов М3C60 (М = K, Rb, Cs) обладают таким свойством. Температура фазового перехода зависит от постоянной решетки фуллерида. Температура сверхпроводящего перехода для системы Rb-Tl-C60 достаточно высока — она превышает 40° K, для системы Cu-C60 - температуру кипения азота. Таким образом, металлофуллерены при простом составе являются одними из самых высокотемпературных сверхпроводников [17]. Для использования в качестве водород-аккумулирующих матриц в настоящее время наиболее перспективными представляются углеродные материалы, особенно в связи с открытием фуллеренов, которые после гидрирования всех двойных связей могли бы содержать до 7.7 % масс. водорода. Однако получить такое соединение пока никому не удалось. Получаемые гидриды фуллеренов C60Hx (максимальный состав - C60H36) содержат до 6 % масс. водорода. Эффект нелинейной прозрачности фуллеренсодержащих растворов и соединений открывает возможности их использования в качестве основы оптических затворов - ограничителей интенсивности лазерного излучения видимого и ближнего инфракрасного диапазонов. Пороговая интенсивность, характеризующая оптический затвор на основе фуллеренов, в несколько раз ниже соответствующего значения для материалов, традиционно используемых в подобных целях (индантрон, фталоцианинат алюминия и др.). Для C60 область оптического ограничения лежит в диапазоне длин волн 400-700 нм. Области оптического ограничения более высоких фуллеренов (C70, C78, C84) лежат в видимой и ближней инфракрасной областях. Важным свойством фуллеренсодержащих оптических ограничителей является их быстродействие - порядка фемтосекунд. Фуллериты обладают фотопроводимостью в спектральном диапазоне, оптимальном для создания солнечных элементов. Спектр фотопоглощения фуллеритовых плёнок лежит в диапазоне длин волн от 280 до 680 нм, а квантовый выход (вероятность образования электрон-ионной пары при поглощении одного фотона) составляет 0.9. Необходимо отметить, что сами по себе фуллерены являются токсичными веществами, например, фуллерен C60 приводит к окислительному разрушению липидов. Это было выяснено изучением влияния коллоидного раствора C60 на мозг рыб, а затем и на клетки человека in vitro. Однако в еще одной работе было выяснено, что при химической модификации фуллеренов гидроксильными или карбоксильными группами, фуллерен становится гораздо менее вредным. Данные группы повышает гидрофильность фуллерена, вследствие чего он становится водорастворимым. Было найдено, что чем больше фуллерен растворим в воде, тем менее токсичным он является. Например, соединение C60(OH)24 не проявляет токсичности, даже при максимально возможной концентрации [18].
В начале семидесятых годов независимо друг от друга в теоретических работах советских химиков Д. Бочвара и Е. Гальперн и японского физика Е. Осава обсуждалась возможность существования полиэдрических кластеров углерода, и прогнозировались некоторые их свойства. В 1985 году эти предположения были экспериментально подтверждены Р. Керлом, Г. Крото и Р. Смолли. При исследовании масс-спектров паров графита, полученных при лазерном облучении твердого образца, авторы обнаружили пики, соответствующие массам 720 и 840. Они предположили, что данные пики отвечают индивидуальным молекулам С60 и С70 и выдвинули гипотезу, что молекула С60 имеет форму усеченного икосаэдра симметрии Ih, а С70 – более вытянутую структуру эллипсоидного типа симметрии D5h. Вслед за этим немедленно появилось сообщение, в котором на основании наблюдения в масс-спектрах паров графита, допированного атомами La, пика , был сделан вывод о возможности внедрения во внутреннюю полость сфероидной молекулы С60 атома лантана [19] с образованием эндоэдрального комплекса LaC60. Оба эти предположения в дальнейшем блестяще подтвердились. В 1990 году В. Кречмером и Д. Хаффманом был предложен способ получения фуллеренов в макроскопических количествах. С этого момента начался "фуллереновый бум", а поток публикаций об их удивительных свойствах резко возрос.
- Эндометаллфуллерены
Эндоэдральные углеродные кластеры (эндометаллофуллерены MC2n), содержащие атомы металла внутри фуллереновой молекулы, являются производными фуллеренов и в настоящее время выделились в отдельную область научных исследований и представляют особый интерес. Образование подобных соединений наиболее характерно для молекулы фуллерена C82 с металлами 3-й группы (Sc, Y, La) и лантаноидами. Известны также эндометаллофуллерены и с другими углеродными кластерами: C60, C70, C76, C78, C80, C84 и другие. Эндометаллофуллерены представляют собой совершенно новый тип углеродных кластеров, существенно отличающихся от полых фуллеренов. Атом металла, внедренный внутрь [20] фуллереновой молекулы, значительно изменяет ее электронные свойства. В случае LaC82 три электрона от металла переходят на фуллерен, образуя комплекс La 3+C82 3- рисунке 6.
Рисунок 6 – Эндометаллофуллерен LaC82 (15 атомов углерода из 82-х убраны для наглядности)
В отличие от полых фуллеренов, которые обладают выраженными акцепторными свойствами, для эндометаллофуллеренов помимо акцепторных свойств характерны и донорные. Эндометаллофуллерены могут содержать один или несколько атомов металлов внутри фуллеренового каркаса и быть парамагнитными или диамагнитными соединениями. Уникальная структура эндометаллофуллеренов и разнообразие их свойств в зависимости от внедренного металла и фуллерена вызывают большой интерес к ним в плане изучения их химических и физических свойств. Можно ожидать, что эндометаллофуллерены [21] послужат основой для создания новых материалов с особыми свойствами: сверхпроводники, органические ферромагнетики, лазерные и сегнетоэлектрические материалы, фармацевтические и радиофармацевтические препараты и т.п. Однако эндометаллофуллерены до сих пор мало изучены. В литературе практически отсутствуют данные о их химических и физических. Главной причиной такого положения является ограниченная доступность эндометаллофуллеренов, что связано с проблемами их синтеза и выделения в значительных количествах.
Молекулы фуллеренов, в клетку которых заключены один или несколько атомных частиц (атомов или молекул), получили название эндоэдральных соединений (или эндоэдралов). Для обозначения таких молекул используется формула МmСn где М — инкапсулированный атом или молекула, а нижние индексы m и n указывают на число таких атомов и атомов углерода в молекуле фуллерена соответственно. Рекомендуемое IUPAC название для LaC82 звучит следующим образом “ fullerene-incar-lanthanum” и записывается в виде iLaC82.
Особенность электронной структуры эндоэдральных металлофуллеренов, связанная с передачей валентных электронов металла фуллереновой оболочке, фундаментальным образом отражается на свойствах этих соединений. Так, эндоэдральные фуллерены, содержащие атомы металлов второй группы, имеют диамагнитные свойства, поскольку инкапсулированный двухзарядный ион металла содержит только полностью заполненные электронные оболочки, а спиновые моменты валентных электронов, находящихся на внешних орбиталях фуллереновой оболочки, полностью скомпенсированы.[22] Это объясняет отсутствие какого-либо сигнала в спектрах ЭПР. Напротив, эндоэдральные фуллерены, содержащие атомы металлов третьей группы, обладают парамагнитными свойствами, поскольку инкапсулированный трехзарядный ион металла передает три электрона на фуллереновую оболочку.
В эндометаллофуллеренах газокинетический размер инкапсулированного атома значительно меньше внутреннего размера фуллереновой оболочки. Отсюда возникает вопрос о положении атома внутри углеродного кластера. Исследования показали, что смещение металла относительно геометрического центра молекулы, связано с передачей валентных электронов от инкапсулированного атома [23] на внешнюю поверхность фуллереновой оболочки и возникающим сильным электростатическим взаимодействием образующегося при этом положительного иона с отрицательно заряженной оболочкой.
Смещение равновесного положения инкапсулированного атома относительно геометрического центра фуллереновой оболочки определяет наличие у таких молекул довольно значительного постоянного дипольного момента. Так, согласно оценке, выполненной авторами работ, дипольный момент молекулы YC82 составляет 2,5 D. Значение дипольного момента молекулы LaC82 оценивается 3¸4 D. Наличие у эндоэдральных металлофуллеренов постоянного дипольного момента придает материалам на основе этих соединений особые свойства, связанные с возможной ориентацией молекул в кристалле и возникновением постоянной поляризуемости. Такие кристаллы должны обладать сегнетоэлектрическими свойствами и могут найти интересные применения в электронных устройствах.
Перестройка электронной структуры эндоэдральных металлофуллеренов, связанная с переходом валентных электронов металла на внешнюю по отношению к оболочке область, отражается на таких электронных характеристиках молекулы фуллерена, как ее потенциал ионизации и сродство к электрону. Это можно проиллюстрировать результатами квантово-химических расчетов, представленными в таблице 1. Как видно, инкапсулирование атома металла в молекулу фуллерена, с одной стороны, приводит к снижению потенциала ионизации, с другой стороны, энергия сродства эндоэдралов заметно выше, чем пустых фуллеренов.
Таблица 1 – Результаты квантово-химических расчетов
|
Фуллерен |
IP,эВ |
EA,эВ |
Заряд на атоме металла |
||
|
нейтральной молекуле |
катионе |
анионе |
|||
|
Sc@C82 Y@C82 La@C82 C60 C70 C82 |
6,45 6,22 6,19 7,78 7,64 6,96 |
3,08 3,20 3,22 2,57 2,69 3,37 |
2,16 2,59 2,92 |
2,18 2,61 2,97 |
2,18 2,60 2,90 |
Основные отличия эндоэдральных металлофуллеренов от полых фуллереновых молекул связаны с двумя главными особенностями их структуры. Первая из этих особенностей обусловлена нецентральным положением инкапсулированного атома металла в клетке фуллерена, вследствие чего молекула эндоэдрального фуллерена имеет постоянный дипольный момент, наличие которого сказывается на макроскопических характеристиках соответствующего фуллерита. Потенциал взаимодействия молекул, обладающих дипольным моментом, не является сферически симметричным, поэтому составленный из таких молекул кристалл должен обладать сильно выраженными анизотропными свойствами. Вторая особенность связана с зарядовым состоянием инкапсулированного атома и с переходом валентных электронов от этого атома на внешнюю поверхность молекулы фуллерена. Наличие электронов на наружной поверхности фуллереновой оболочки определяет характер межмолекулярного взаимодействия [24] в кристалле, в которое наряду с ван-дер-ваальсовым дает определенный вклад и ковалентный механизм.
Постоянный дипольный момент молекул эндоэдральных металлофуллеренов обусловливает несферический характер их взаимодействия между собой. Это, в свою очередь, способствует образованию протяженных структур (агрегатов), содержащих некоторое количество подобных молекул. О прямом наблюдении подобных структур сообщалось, в частности, в работе, где с помощью сканирующего туннельного микроскопа, оснащенного полевым ионным микроскопом, изучалось поведение молекул YC82 на поверхности Cu(111), имеющей плотность дефектов менее 0,1%. Наблюдения проводились в условиях вакуума глубиной 6´10-11 Торр. Как следует из результатов наблюдений, выполненных с помощью STM, молекулы на поверхности подложки сохраняют подвижность и имеют тенденцию к адсорбции на краях террасы, образованной на поверхности. Это отличает медную подложку от кремниевой Si(111) и Si(100), на которой положения молекул эндофуллеренов фиксированы. Эндофуллерены YC82 на поверхности подложки образуют кластеры (YC82)n (n=2¸6), в частности димеры, даже на самой начальной стадии напыления, когда поверхностная плотность молекул весьма невелика. Показано, что расстояние между молекулами в димере (1,12 нм) меньше, чем соответствующее ван-дер-ваальсово значение (1,18 нм). Это указывает на наличие сильного, не ван-дер-ваальсова взаимодействия между молекулами димера, которое связано с дипольным моментом (~ 2,5 Д). Тем самым эндоэдральные фуллерены проявляют способность к ориентационному выстраиванию, что придает кристаллам [25] на их основе анизотропные свойства, и делает их перспективным материалом с точки зрения приложений.
Как известно, фуллеренам присущ фазовый переход ориентационного разупорядочения, который сопровождается размораживанием вращения молекул относительно оси симметрии. Этот фазовый переход связан с некоторым отклонением формы молекул фуллеренов от идеальной сферы и соответствующим отличием потенциала межмолекулярного взаимодействия от сферически симметричного. В случае фуллерита С60 указанный переход наблюдается при Т ~ 260 К и характеризуется теплотой перехода Dh = 850 К. В случае эндоэдральных металлофуллеренов, которые характеризуются более высокой энергией межмолекулярного взаимодействия и более значительным отклонением потенциала взаимодействия от сферически симметричного, данный переход должен, казалось бы, происходить при более высокой температуре и обладать более высоким тепловым эффектом. Этот вывод, однако, противоречит результатам измерений, [26] согласно которым в кристалле 139Се 140Lа С80 фазовый переход, сопровождаемый размораживанием вращения молекул, наблюдается при Т=160 К и характеризуется тепловым эффектом 380 К. Возможно, причина указанного расхождения состоит в том, что при вращении молекул в кристалле не нарушается их ориентация вдоль оси расположения инкапсулированных атомов. В таком случае в кристалле рассматриваемого типа при температуре выше или порядка комнатной должен наблюдаться еще один фазовый переход, обусловленный нарушением продольной ориентации молекул. Тем самым вопрос о связи между характером межмолекулярного взаимодействия и динамикой молекул эндометаллофуллеренов в твердофазном состоянии требует дополнительных исследований.
Интересная особенность эндоэдральных соединений связана еще с тем, что атом, заключенный в фуллереновую оболочку, практически теряет свои индивидуальные химические свойства. На это указывают, в частности, результаты одного из первых экспериментов по установлению химических характеристик эндоэдральных фуллеренов. В этой работе сравниваются химические активности по отношению к реакции с молекулой N02 эндоэдральной молекулы YС60 полученной методом лазерного испарения, и экзоэдральной молекулы YС60, полученной в масс-спектрометре ионно-циклотронного резонанса с фурье преобразованием. Как показывают измерения, атом иттрия, входящий в состав экзоэдрального соединения легко окисляется с образованием YO, в то время как эндоэдральный комплекс сохраняет стабильность даже при повышении концентрации N02 в 1000 раз. Этот результат, который дополнительно подтверждает эндоэдральную структуру молекулы.[9,26]
1.6 Пористый оксид алюминия
Ещё одним вариантом наносистем является пористый оксид алюминия. Его отличает сравнительно простая методика синтеза и следовательно низкая стоимость. Также важно отметить, что в процессе синтеза пористого оксида алюминия мы получаем не единичные наночастицы, а упорядоченную матрица наночастиц. Данная технология становится более значительной, при разработке методики заполнения пор другими материалами. В частности в нашей работе это металл (медь).
При электрохимическом травлении алюминия, оксид алюминия образуется на аноде в соответствии с реакцией [10]:
(7)
При этом на катоде выделяется водород:
(8)
Количественной мерой окислительной способности окислителя (и одновременно восстановительной способности его восстановленной формы) является электрический потенциал электрода φ (электродный потенциал), на котором одновременно и с равными скоростями протекают полуреакция его восстановления и обратная ей полуреакция окисления соответствующей
(9)
где E – потенциал электрода;
R-универсальная газовая постоянная;
T –температура;
z – зарядовое число электрода;
F – постоянная Фарадея;
[red] – концентрация восстановителя;
[ox] – концентрация окислителя;
E0 –стандартный электродный потенциал.
С учетом параметров реакции (1) электродный потенциал Е может быть записан в виде:
(10)
Выражение (4) показывает, что реакция на аноде (Al) термодинамически зависит от значения pH, которое определяется электролитом и температурой.
Уравнения (3) и (4) являются термодинамическими, то есть они не могут объяснить ни возникновение пористой, ни тем более упорядоченной пористой структуры. Одной из наиболее успешных моделей, объясняющих [27] образование упорядоченных структур, является модель механического напряжения.
Модель базируется на следующих положениях:
- Окисление происходит во внешнем слое металла посредством перемещения кислородосодержащих ионов O-2 и OH- из электролита.
- Растворение оксидной пленки происходит благодаря реакции гидратации сформированного оксидного слоя.
- В случае образования оксида барьерного типа все ионы Al+3 достигающие границы оксид-электролит вносят вклад в формировании оксидной пленки. С другой стороны, пористый оксидный слой образуется, когда ионы Al+3 проникают сквозь оксидную пленку.
- Поры растут перпендикулярно поверхности при сбалансированности процессов роста оксида на границе оксид-металл и растворения на границе оксид-электролит.
- Сформированный оксид имеет химическую формулу Al2O3. Поэтому атомная плотность алюминия в оксиде алюминия в два раза меньше плотности металлического алюминия. Это означает, что объем анодированного алюминия увеличивается примерно в два раза по сравнению с исходным.
- Увеличение объема приводит к сжатию во время образования оксида на границе оксид-металл. Увеличение в вертикальном направлении толкает стенки пор вверх.[11,12,13]
На основе данной модели рассчитывается коэффициент объемного увеличения ξ:
, (11)
где – , и - плотность алюминия, плотность пористого алюминия и весовая доля ионов алюминия соответственно;
V – объем;
W – вес алюминия и оксида алюминия.
Коэффициент ξ определяет механические напряжения, возникающие в пленке, и, следовательно, процесс формирования упорядоченных либо неупорядоченных пор. Если механическое напряжение слишком велико (ξ ~ 2), то поры образовываться не будут. При слишком малом механическом напряжении (ξ<1.2) силы, обеспечивающие упорядочение, будут малы, а следовательно сформируется массив неупорядоченных наноструктур. Случай умеренных сил (ξ≈1.2) обеспечивает рост упорядоченных структур. При выполнении неравенства 1.3 < ξ < ξмах рост упорядоченных доменов оксида алюминия будет продолжаться до тех пор, пока не исчезнет по причине отталкивающих взаимодействий. Можно заключить, что наиболее хорошо упорядоченные структуры на основе оксида алюминия получаются при коэффициенте увеличения объема ξ равном 1.2. [12,27]
Рассмотрим параметры анодирования, влияющие на образование упорядоченных наноструктур.
Напряжение U является одним из наиболее важных параметров, влияющих на упорядоченность наноструктур. Расстояние между порами Dint пропорционально приложенному напряжению, с коэффициентом пропорциональности 2.5 ≤ k ≤ 2.8 (nm/V).
. (12)
Тип и концентрацию электролита необходимо подбирать для данного напряжения для того, чтобы получить рост упорядоченных наноструктур. Травление алюминия в серной кислоте проводится при низком напряжении (~40 В), в щавелевой кислоте при среднем (30÷120 В) и в фосфорной кислоте при высоком (80÷200 В). Это ограничение вызвано электропроводностью и значением pH электролита. К примеру, если проводить [28] травление алюминия в серной кислоте при высоком напряжении, то произойдет пробой оксидной пленки образца, так как электропроводимость серной кислоты высока. Значение pH электролита определяет диаметр пор. Чем меньше pH, тем меньше диаметр пор.
Во время анодирования температура должна быть меньше комнатной, чтобы избежать растворения формирующегося оксида кислотным электролитом. Например, травление в щавелевой кислоте при напряжении 40 В лучше проводить при температуре 5÷18OC, а в случае фосфорной кислоты и напряжения 195 В значение температуры травления должно находиться в пределах 0÷20С.
Еще одной причиной для поддержания минимально возможной температуры является необходимость избежать локального нагревания дна пор во время процесса анодирования. Локальный нагрев [29] приводит к возникновению негомогенного электрического поля, которое в свою очередь приводит к локальному пробою оксидной пленки. При слишком низкой температуре электролит может замерзнуть, в этом режиме также замедляется формирование пор. [15,16]
В зависимости от условий реакции, в частности, типа электролита, температуры, электродного потенциала, могут быть получены два вида анодных пленок. Барьерный тип пленок может формироваться в полностью нерастворимых электролитах (5 < pH < 7), таких как борная кислота, борат аммония и тетраборат аммония в этиленгликоле. Пористый тип пленок может быть создан в мало растворимых электролитах, таких как серная, фосфорная, и щавелевая кислоты. В этом случае структура оксида может быть представлена в виде трубчатых пор, окруженных слоем оксида барьерного типа (барьерным слоем). Толщина барьерного слоя может быть определена как половина расстояния между порами (Dint=2Db где Db толщина барьерного слоя). [14,28]
Толщина пленки оксида алюминия барьерного типа определяется, в основном, приложенным напряжением. Максимально достижимая толщина для плёнок барьерного типа из оксида алюминия соответствует напряжению пробоя в диапазоне 500-700 В, и равна примерно 1мкм. При большем напряжении происходит диэлектрический пробой плёнки.
С другой стороны, так как толщина пористого оксида алюминия зависит от времени, то вследствие этого могут быть получены более толстые пористые плёнки. Время анодирования, плотность тока и тип электролита являются важными параметрами в определении толщины пористого слоя оксида алюминия. При повышении температуры [ 30] соответствующая плотность тока также увеличивается. Но это не означает, что более высокая больше, чем скорость образования оксида, то пленка может исчезнуть. Фактически это приведет к электрохимической полировке алюминия, а плотность тока приводит только к увеличению толщины пленки.
При возрастании плотности тока происходит также изменение соотношения процессов растворения и образования оксида на границе раздела электролит-оксид.
Качественно процесс формирования пористых наноструктур оксида алюминия представлен на рисунке 7.
На поверхности чистого алюминия с течением времени образуется оксидная пленка барьерного типа (А), которая состоит из непроводящего оксида и достаточно однородно покрывает поверхность алюминия. В электрохимической ячейке электрическое поле локализуется на неоднородностях поверхности оксидной пленки (Б), что приводит к растворению формирующего оксида тем более интенсивного, чем выше неоднородность поля. Таким образом, в областях наибольшей неоднородности поверхности происходит рост пор (В), усиливающийся как при увеличении температуры, так и при усилении поля. Между соседними порами в процессе роста имеет место конкуренция, которая по прошествии некоторого времени приводит к стабилизации процесса и упорядочению роста пор (Г).[31,32]
Рисунок 7 – Процесс образования двумерных наноструктур пористого оксида алюминия
1.7 Факторы, влияющие на рост анодной окисной пленки на алюминии
Основными процессами, протекающими при анодной поляризации алюминия в серной кислоте, являются:
1) электрохимический процесс образования окисла в барьерном слое;
2) химический процесс растворения окисла под действием электролита;
3) побочные процессы, как например, газовыделение, гидратация окисла, внедрение анионов в состав окисла [33].
Теоретическое количество окисла алюминия, возникающего при анодировании на единице поверхности (при условии, что образованный окисел не растворяется и отсутствуют побочные процессы), согласно закону Фарадея, зависит от количества пропущенного электричества, т. е. от произведения плотности тока на продолжительность электролиза:
(13)
где Р — теоретическое количество окиси в г/дм2;
i — плотность тока в а/дмг;
τ— время анодирования в ч;
с — электрохимический эквивалент анодного окисления алюминия, представляющий собой число граммов А1203, образующейся при прохождении 1 а·ч количества электричества, и численно равный 0,635 г/а·ч.
Исходя из изложенных представлений о механизме роста анодных окисных пленок пористого типа, можно было бы предположить образование окисной пленки неограниченной толщины. Однако формирование пленки возможно до сравнительно небольших толщин, после достижения которых рост пленки практически прекращается. Предельные толщины анодных пленок удовлетворительного качества определяются в каждом конкретном случае специфическими условиями анодного процесса [34].
Пленки толщиной до 10—15мк получают по так называемому нормальному режиму анодирования при комнатной температуре и плотности тока 1 — 2 А/дм2. Пленки толщиной до 50—100 мк получают главным образом при низких температурах электролита (около нуля или даже ниже) и плотности тока от 2 до 10 А/дм2, а также при комнатных температурах (до 20° С) и постоянной мощности тока или в смесях электролитов. Пленки с максимальной толщиной (150мк и более) можно получить только при двустороннем охлаждении — с внешней стороны пленки через электролит и с внутренней стороны через металл, т. е. с применением так называемого внутреннего охлаждения.
Рисунок 8 – Рост толщины (δ) анодной пленки во времени (τ)
Окисная пленка достигает при анодировании предельной толщины пор вследствие возрастания скорости растворения пленки до скорости ее образования (это наблюдается в условиях недостаточно эффективного охлаждения при анодировании), или вследствие чрезмерного возрастания напряжения и электрического пробоя пленки.
Достижение предельной толщины пленки в этих двух случаях определяется прежде всего тем, что скорость процесса образования окиси алюминия во время анодирования замедляется, за счет усиления побочных электрохимических процессов на аноде, в то время как скорость процесса растворения пленки возрастает вследствие повышения температуры анода. На рисунке 3 прямая 1 изображает [35] теоретический рост толщины пленки под действием проходящего тока (при отсутствии расхода тока на другие процессы), кривая 2 характеризует толщину анодной пленки, растворяемой электролитом. Скорость этого процесса сильно возрастает с повышением температуры электролита [19, 12, 20].
Результирующая кривая 3, полученная как разность кривых 1, 2, характеризует реальный рост толщины окисной пленки. Горизонтальный участок кривой 3 свидетельствует о том, что толщина пленки уже не увеличивается, несмотря на то, что анодирование продолжается — пленка просто как бы передвигается внутрь металла.
Практически невыгодно достигать предельных для данного режима толщин пленки, так как при этом скорость роста пленки все более замедляется, возрастают потери тока на растворение металла и ухудшаются механические свойства пленки. Поэтому на практике время анодирования обычно ограничивают периодом быстрого роста пленки, что всегда будет приводить к некоторому утолщению образца [36,37].
К числу основных факторов, влияющих на характер протекания анодного процесса и свойства получаемых пленок, следует отнести в первую очередь влияние таких факторов, как концентрация и температура электролита и плотность анодного тока. Существует определенный оптимум агрессивности (концентрации) электролита, при котором можно получить пленки предельных толщин. В более агрессивных растворах (например, концентрированных растворах H2S04) барьерный слой не успевает сформироваться, так как сразу же начинает растворяться в кислоте. Однако и в этом случае более обоснованным является предположение, что растворение алюминия осуществляется не путем первичного анодного процесса реакции, но через анодное окисление (1) и последующее химическое растворение окисла. При малой агрессивности раствора (например, при чрезмерно заниженных концентрациях) толщина барьерного слоя приближается к максимальной величине, характерной для электролитов, которые не растворяют окисную пленку. В этом случае способность [38] электролита растворять пленку и образовывать поры сильно уменьшается, что влечет за собой снижение плотности тока, а, следовательно, уменьшение скорости роста пленки ниже допустимого предела или повышение клеммового напряжения до наступления электрического пробоя пленки.
Увеличение плотности тока также возможно лишь в ограниченных пределах, и хотя скорость формирования окисной пленки является, прежде всего, функцией плотности тока, увеличение последней выше допустимого для данных условий предела сопряжено с перегревом анода и, следовательно, может, наоборот, повести к уменьшению предельной толщины пленки и изменить ее свойства и течение анодного процесса в нежелательную сторону [39].
Таким образом, наиболее действенным фактором для повышения предельных толщин анодных окисных пленок является снижение температуры анода
1.8 Заполнение пор металлом
Пористая матрица анодированного алюминия в дальнейшем может заполнятся различными веществами. Например, молекулами красителя при декоративном окрашивании поверхности алюминиевой детали. В нашей работе предложено заполнять поры металлическими наночастицами. Данный процесс лучше всего проводить электрохимическим осаждением металла на пористую матрицу оксида алюминия. Согласно формуле Фарадея масса выделившегося в порах и на поверхности металла определяется как [25]
, (14)
где – постоянная Фарадея;
m — масса осаждённого на электроде вещества в граммах;
Q — полный электрический заряд, прошедший через вещество;
F = 96 485,3383(83) Кл·моль−1 — постоянная Фарадея;
M — молярная масса вещества;
z — валентное число ионов вещества (число электронов на один ион).
Заметим, что — это эквивалентная масса осаждённого вещества.
В простейшем случае постоянного тока электролиза приводит
(15)
Так, например, для электролиза меди из раствора медного купороса с медным анодом электрохимическая реакция имеет вид. Молекулы серной кислоты при растворении в воде диссоциируют на ионы водорода и ионы кислотного остатка:
(16)
При прохождении электрического тока через раствор на электродах протекают следующие реакции:
(17)
Водород выделяется в виде пузырьков на катоде. Нейтральная группа SO4 химически очень активна и вступает во вторичную реакцию. Если электроды изготовлены, например, из платины или никеля, то SO4 реагирует с водой:
(18)
Молекула серной кислоты поступает в раствор, кислород выделяется в виде пузырьков у анода, т.е. вторичная реакция протекает с растворителем.
Таким образом, зная силу тока и время осаждения можно узнать массу металла и оценить объем пор. [21,35,36]
. (19)
Электролиты для меднения
Медный электролит для гальванопластических работ приготовляют на основе кристаллогидрата сульфата меди с добавкой серной кислоты H2SO4, повышающей электропроводность.
Для приготовления медного электролита отвешивают сульфата меди из расчёта 180г на 1л воды. Растворение сульфата меди лучше всего вести в горячей или тёплой воде. После полного охлаждения раствора и его доведения до комнатной температуры электролит фильтруют через ткань и осторожно вливают в него серную кислоту. Серную кислоту важно вливать медленно, тонкой струёй, во избежание быстрого разогревания электролита и разбрызгивания, что может вызвать тяжёлые химические ожоги. В медных сульфатных ваннах содержание серной кислоты поддерживается в пределах 30-35 г/л. Растворимость сульфата меди значительно снижается с увеличением содержания серной кислоты. При наличии повышенного содержания сульфата меди он выкристаллизовывается на стенках ванны и, что хуже на аноде, препятствуя процессу электролиза. Избыток серной кислоты в ванне вызывает хрупкие и недоброкачественные отложения меди из-за включения водорода, интенсивно выделяющегося на катоде, особенно при работе с повышенными плотностями тока. При недостаточной концентрации серной кислоты в электролите [40] образуется рыхлый и пористый осадок меди, непригодный для практических целей.
Кроме сульфата меди и серной кислоты, для повышения качества гальванопластической меди применяют добавки, например спирт, в количестве 8-10г/л. Добавка меди значительно улучшает качество меди, делая её менее кристаллической, более твёрдой и упругой. Добавку меди вводят не более нормы, так как большое количество добавки делает медь хрупкой.
2 Приборы и техника эксперимента
2.1 Электролитическая ванна
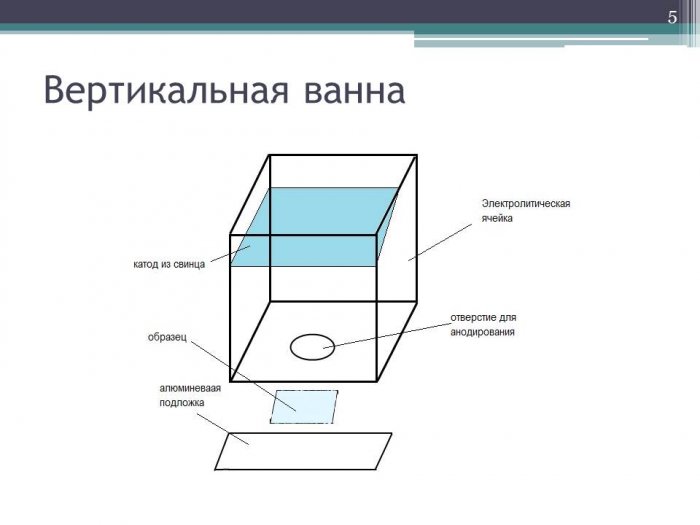
Установка для анодирования пористого оксида алюминия представляет собой прямоугольную электролитическую ванну из материала, не реагирующего с электролитом. В качестве этого материала был использован полиметилметакрилат, который инертен ко многим химическим средам, является диэлектриком и оптически прозрачен. Электролитическая ячейка используется с вертикальным отверстием для анодирования. Ванна используется для проведения электрохимических реакций и может использоваться по двухэлектродной схеме. В ванне предусмотрено горизонтальное расположение анодируемого образца. Сделано это для того, чтобы сделать структуру анодного слоя более регулярной, в отличие от горизонтальной ванны и исключить влияние газообразования на процесс анодирования.
Рисунок 9 – Электролитическая ячейка с горизонтальным анодированием
Установка позволяет проводить анодирование в гальвано и потенциостатическом режиме по 2-х электродной схеме.
Источником питания постоянного тока Б5–49 стабилизировались электрический ток при гальваностатическом режиме или электрический потенциал при потенциостатическом режиме.
Рисунок 10 – Источник питания Б5-49
Катод представляет собой плоскую свинцовую пластинку т.к. свинец не реагирует с выбранными нами электролитами. В качестве анода используется алюминиевая или медная подложка, на которой плотно прилегает алюминиевая фольга. Подложка должна быть очищена и обезжирена для того, чтобы между образцом и подложкой был идеальный контакт. Ванна и подложка плотно фиксируются между собой.
Чтобы получить более четкую проанодированную область только в окошке анодирования желательно смочить зажатую фольгу водой.
При проведении ряда экспериментов, между перегородками в несмоченных водой областях наблюдаются маленькие растворенные дырочки в алюминиевой фольге. Растворение происходит в воздушных пузырьках, заключенных между перегородками. Газ образуется в результате электрохимических реакциях на аноде, который впоследствии может растворить и В случае, когда фольга смачивается водой, попадание образующегося газа в зазор между перегородкой и фольгой уменьшается за счет поверхностного натяжения воды. Смачивание водой так же препятствует попаданию электролита в область, находящуюся между прижатыми пластинками. При затекании электролита в эту область происходит электрохимическая реакция на алюминиевой фольге, которая отображается на осциллограмме в виде небольших спадов напряжения, так как уменьшается плотность тока за счет увеличения анодированной площади алюминиевой фольги. Эти изменения существенно не влияют на процесс анодирования алюминия.
2.2 Используемые растворы и образцы
Анодирование проводилось в водном растворе серной кислоты концентрации 20% (по массе) при заданной температуре. Серная кислота наливалась в воду тонкой струйкой, во избежание быстрого разогрева раствора и его разбрызгивания, которое может привести к химическим ожогам. Время анодирования и сила тока варьировались. Процесс происходил до полного преобразования алюминия в пористый оксид или частичного (т.е. когда анодный слой составляет 50-80% от толщины фольги).
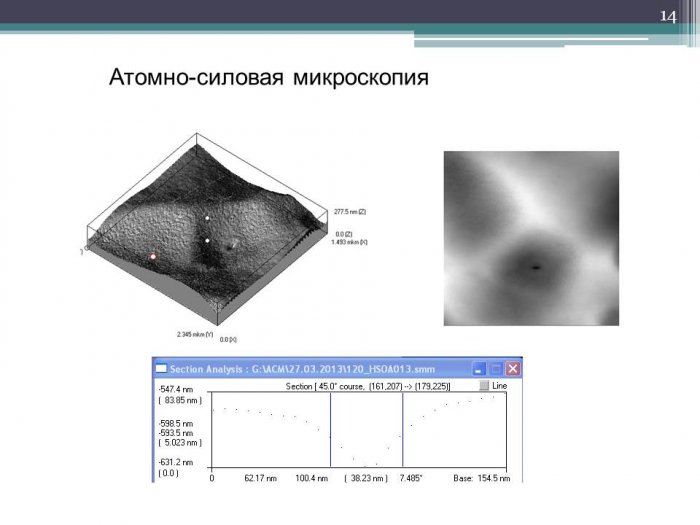
2.3 Измерения на атомно-силовом микроскопе
Микроскопическое исследование препаратов проводилось на атомно-силовом микроскопе ССМ–2000 (производитель OAOПРОТОН – МИЭТ, Россия) в контактном режиме в воздушной среде.
Микроскопы сканирующие зондовые ССМ-2000 предназначены для измерений геометрических и физических параметров топографии поверхности образцов с нанометровым пространственным разрешением безихвакуумирования.
Действие микроскопов сканирующих зондовых СММ-2000 основано на подводе к исследуемой поверхности зонда с иглой до регистрации определенного уровня сигналов взаимодействия зонда с поверхностью и далее сканировании поверхности с регистрацией и поддержанием сигналов взаимодействия зонда с поверхностью на заданном оператором уровне за счет подвода или отвода зонда от поверхности с компьютерной записью и дальнейшей визуализацией положений зонда и уровней сигналов взаимодействия зонда с поверхностью при сканировании, отражающих геометрические и физические параметры топографии поверхности образцов с нанометровым пространственным разрешением. Фото микроскопа представлено на рисунке 11.
Рисунок 11 – Фотография микроскопа сканирующего зондового СММ-2000
При микроскопии использовались зонды для контактной атомно-силовой микроскопии MSCT-AUNM (Veeco, США), с жесткостью балки 0,33 Н/м и радиусом кривизны зонда 10 нм. Количественный морфометрический анализ проводился с использованием штатного программного обеспечения микроскопа.
Для приготовления образцов сухая масса исходного вещества в количестве 1,5 г помещалась в стеклянные флаконы, куда так же вносили по 10 мл дистиллированной воды. После чего в течение 30 минут производилась обработка образцов ультразвуком частотой 35 кГц в источнике ванного типа (ЗАОПКФ «Сапфир», Россия). После ультразвуковой обработки, полученная суспензия помещалась в центрифугу (ListonC2204 Classic), где при 4000 оборотах в течение 75 секунд. Крупнодисперсная фракция осаждалась, а полученный супернатант в объеме 15 мкл наносился на поверхность свежесколотой слюды.
Микроскопы сканирующие зондовые СММ-2000 работают в режиме атомно-силового микроскопа, если регистрируемым и поддерживаемым на заданном уровне сигналом является сигнал отгиба или амплитуды колебаний зонда-кантилевера, выполненного в виде упругой балки с иглой.
2.4 Подготовка образцов
В качестве исходного материала использовалась алюминиевая фольга (с процентным содержанием основного вещества не менее 99,5 %) толщиной 40 мкм. Далее образец проходил ряд обязательных процедур, мы перечислим их здесь в прямом хронологическом порядке.
Отжиг
На первом этапе образцы подвергались рекристаллизационному отжигу в муфельной печи при температуре 4500 С, т.е. нагреву металла до температур выше начала кристаллизации, и временем выдержки 40 – 60 минут с последующим медленным охлаждением со скоростью 30оС/ч. Рекристаллизационный отжиг применяется для снятия эффекта упрочнения, наклепа и уменьшения плотности дефектов кристаллической решетки, таких как вакансии и дислокации. В процессе такого отжига происходит образование зародышей новых зерен и последующий рост этих зародышей. Постепенно старые деформированные зерна исчезают. Количество дефектов в кристаллической решетке уменьшается, наклеп устраняется, и металл возвращается в исходное состояние. В результате кристаллическая решетка алюминия приобретает первоначальное строение – строение гранецентрированной кубической решетки (ГЦК). Особенность муфельной печи заключается в том, что нагрев идёт не равномерно на все плёнки. В центре печи температура установленная, а ближе к краю температура уменьшается из-за того, что там находится дверца, которая закрывается не герметична.
Химическая очистка
Металлические изделия подвергаются воздействию окружающей среды, в результате чего их поверхность покрывается термической окалиной, продуктами коррозии. Этот инородный слой препятствует доброкачественному выполнению последующих технологических операций. Перед осаждением на изделия металлических или оксидных покрытий поверхность их должна быть очищена от указанных химических соединений. Для этой цели используют щелочное травление.
В разведённый раствор NaOH, концентрации 40г/л, нагретый до температуры 60 – 70 оС опускается образец на 20–30 секунд. Затем промывается в дистиллированной воде 1 минуту. Данная операция повторялась 3–4 раза. При такой температуре происходит хорошее растворение оксидного слоя. В результате травления алюминия в едком натрии образуется алюминат натрия и выделяется водород. Интенсивное выделение водорода свидетельствует о быстром растворении алюминия и может служить сигналом для выгрузки деталей из раствора.
Химическая полировка
На алюминиевой фольге после травления остаётся тёмный налёт из нерастворимых составляющих сплава(медь, марганец, железо и т.д.). Осветление, т.е. удаление налёта, производится в смеси кислот при химической полировке (при помощи 25–30% азотной кислоты).
В раствор, содержащий 65% (по объему) ортофосфорной кислоты, 25% серной кислоты и 10% азотной кислоты нагретый до температуры 1000 – 1100 С, опускается образец на 30 – 40 секунд. Затем промывается в дистиллированной воде 1 минуту. Операция повторяется 5 – 6 раз. При погружении алюминиевой фольги в раствор кислот выделяется газ Н2; в кислоте пассивная пленка оксида алюминия растворяется и катионы Н+ получают доступ к алюминию и растворяют его.
В результате химического травления и осветления алюминиевая фольга имеет глянцево – матовую гладкую поверхность. Такая предварительная обработка приводит к более упорядоченному зарождению пор и впоследствии при анодировании к регулярной гексагональной структуре пор оксида алюминия. Полученный образец готов к анодированию в электрохимической ячейке.
3 Экспериментальная апробация технологии синтеза композитных наноструктур «пористый окид - металл»
3.1 Получение пористого оксида
Анодирование проводилось в водном растворе серной кислоты концентрации 20% (по массе) при заданной температуре. Время анодирования определялось условиями анодирования. Процесс происходил до полного и частичного преобразования алюминия в пористый оксид алюминия. Плотность тока, проходящего через образец варьировалась, и для различных образцов составляла от j = 1 А/дм2 до j = 5 А/дм2.
Анодирование проводилось при комнатной температуре с перемешиванием электролита мешалками. При анодировании температура оставалась практически неизменной. В нашем эксперименте получения пористых оксидных пленок (алюминиевая фольга имеет небольшую толщину 40 мкм) охлаждение было не нужно, так как тепло с анодируемой фольги хорошо отводилось за счет теплоотдачи с большой площади неанодируемой области фольги. Помимо температуры варьировался ток и напряжение. Из прошлых работ, мы получили данные, что анодирование лучше проводить при напряжении . Токи изменялись в пределах от I=25mA до I=75mA.
При напряжении и токе время сквозного анодирования составляло . При и токе , время сквозного анодирования - . Мы выбрали самое оптимальное соотношения тока и напряжения , .
Рисунок 12 – Образец сквозного анодирования при I=50 mA, U=40 B
При таких показателях тока и напряжения, время сквозного анодирования составило . Нужно отметить, что все эксперименты проходили при комнатной температуре.
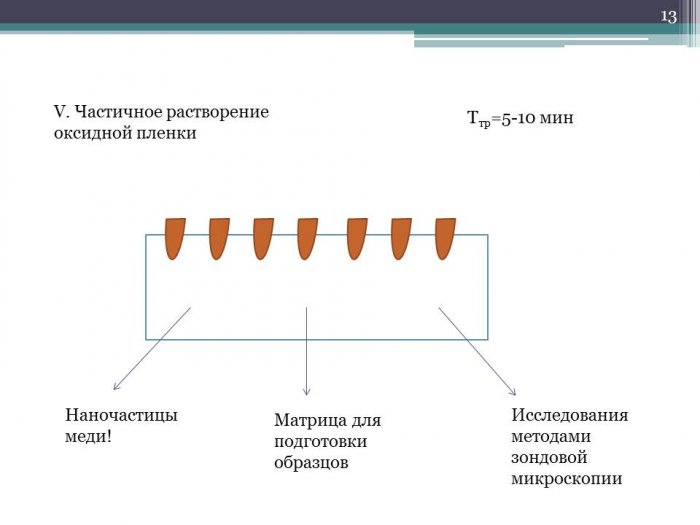
Следующим этапом стало частичное анодирование. Экспериментально было выбрано необходимое время частичного анодирования - 35 минут, при этом доля прореагировавшего металла составляет 80-85 процентов.
Рисунок 13 – Образец частично проанодированного алюминия
Частично проанодированные образцы, изображенные на рисунке 13, далее используются для электрохимического осаждения металла в поры оксидного слоя. В этом случае остаточный слой металла под оксидной матрицей выступает в качестве электрода (катода) при электрохимической реакции.
3.2 Электрохимическе осаждения металла
Электрохимическое осаждение металла позволяет получать на дне оксидной поры металлические наночастицы электролизом водного раствора соли металла.
Подготовка образца
Пленка пористого оксида алюминия по завершению процесса анодирования может быть использована для электрохимического осаждения без дополнительной подготовки, за исключением промывки в дистиллированной воде. Однако в этом случае эффективность заполнения пор наночастицами будет низкой, из-за малого диаметра пор. Поэтому, рекомендуется перед процедурой заполнения пор провести химическое травление оксидной пленки в водном растворе Cr2O3 при температуре 50-60 оС или в растворе при температуре 100-110 оС в течение 3-5 минут, что позволяет увеличивать диаметр полученных пор. Если образец после анодирования хранился более 1-2 дней, рекомендуется провести повторное травление в растворе Cr2O3 при температуре 50-60 оС при температуре 100-110 оС в течение 1-2 мин.
Подготовка рабочего раствора заполнителя
В данной методике нами используются растворы соли металла с концентрацией .
Геометрия установки
Электрохимическое осаждение осуществлялось в электролитической ячейке для горизонтального анодирования. Между отверстием и подложкой помещается образец пористой пленки, ёмкость и подложка герметично соединяются между собой, так, что контакт растворов имеет место только через поры оксидной пленки.
Ход реакции
Если в качестве рабочего раствора заполнителя использовать раствор соли металла (в наших экспериментах CuSO4), и в качестве катода использовать алюминиевый образец, на поверхности которого сформирована пористая матрица, то в ячейке будет протекать реакция электролиза, причем выделение металла из раствора будет происходить главным образом в порах.
Был проделан ряд экспериментов, для определения оптимальных условий заполнения в поры. И выяснилось, что поры лучше всего заполняются при токе 25mA, напряжении 40B, затратив на это времени всего 15 секунд. При увеличении времени, медные частицы прилипают к образцу, и создаётся медная матрица. (t=5 минут). При гальваностатическом режиме (стабилизация по току), напряжение остаётся постоянным и составляет порядка 4-6B. Если увеличивать ток, то медь осаждается на образцы значительно быстрее, но не прилипает к анодированной поверхности (очень легко счищается пальцами).
Рисунок 14 – Образец пористого оксида алюминия с осажденной медью
Таким образом, мы пришли к выводу, что для нас оптимальными режимами заполнения являются следующие:
– для осаждения металла в порах и получения наночастиц меди.
Оценим массу меди выделившейся в порах
. (20)
Объем медных наночостиц при этом ,
см.3 (21)
Очевидно, что он по порядку корреллирует с объемом пор.
В принципе данная техника может служить еще одним (правда косвенным) методом оценки пористости оксидного слоя.
Рисунок 15 – Образец пористого оксида алюминия с введённой в поры медью
– для получения медной матрицы.
Рисунок 16 – Образец анодированного алюминия с медной матрицей
3.3 Перспективные наносистемы, получаемые на основе
пористого оксида заполненного металлом
Полученный образец пористого оксида алюминия с заполненным в поры металлом вытравливается в растворе с концентрацией 250 г/л до тех пор, пока не растворится медь. После растворения меди этот раствор нейтрализуется кислотой до выпадения в остаток соли . В этот раствор добавляется капля тритон X100 (Поверхностно-активное вещество), для того, чтобы наночастицы меди не коагулировали. Полученный после нейтрализации раствор, переливается в пробирку, после чего взбивается в ультразвуковой ванне. После этого, для осаждения тяжёлых частиц меди на дно пробирки, раствор центрифугируется. Наночастицы, в свою очередь, остаются плавать в растворе.
Для того чтобы убедиться, что в этом растворе находятся наночастицы, необходимо снять спектр поглощения на спектрофотометре T70. За базовую линию брался нейтрализованный кислотой раствор щелочи , концентрацией 250г/л., с добавлением ПАВа.
Рисунок 17 - Спектр поглощения раствора наночастиц меди
Этот график полностью совпадает с теоретическим графиком спектра наночастиц меди, полученным в журнале «Квантовая электроника» - П.В. Казакевич, В.В. Воронов, А.В. Симакин, Г.А.Шафеев 34 №10, 2004. (Образование наночатиц меди и латуни при лазерной абляции в жидкости).
а) меди и б) латуни при лазерной абляции в жидкости в растворах: 1-этанол, 2-ацетон, 3-вода
Рисунок 18 – Спектр поглощения образование наночастиц
Для того чтобы убедиться, что на нашем графике нет никаких ошибок, и пик реальный, а не погрешности прибора, был снят график оксида алюминия без наночастиц меди. Как видно на этом графике, спектры сильно отличаются. И наш график спектра поглощения наночастиц меди идентичен тем, которые получались в предыдущих работах.
Рисунок 19 – Спектр поглощения Al2O3 + Cu nanoparticles и базовой линии Al 2O3
Технология получения металлических наноматриц варианты использования.
Полученный образец с металлической наноматрицей вытравливается в щёлочи , с концентрацией 250 г/л. Медная пластинка не реагирует с щёлочью, поэтому вытравливается только алюминий и оксид алюминия. Так как, порах остаются медные наночастицы, то они растворяются, и в следствие этого получается медная пластинка, со стороны алюминия, имеющая медные нанопалочки. Это структуру можно просмотреть на АСМ.
Метод экспресс-контроля наноструктурированных медных поверхностей
Синтез композитных систем на основе пористых матриц анодированного алюминия с внедренными в поры металлическими наночастицами представляет собой сложную задачу, интересную как с фундаментальной физической точки зрения, так и со стороны возможного практического применения данных метаматериалов. Крайне важно при этом иметь прямые методы, позволяющие надежно исследовать полученную структуру, измерять ее размерные характеристики, регулярность и т.д.
Наиболее распространенными и часто применимыми, на сегодняшний момент, являются методы атомно-силовой микроскопии. Однако, не смотря на ряд преимуществ, эти методы нельзя считать универсальными¸ так особенностью данных методов является их высокая локальность, так как информация об объекте снимается с практически точечной области, и не несет информации о структуре объекта в целом. При этом не совсем корректно считать метод АСМ-микроскопии прямым, так как сигнал о рельефе поверхности получается опосредованно, через датчики обратной связи сегнетоэлектрических микропередвижек, или сигналы с оптического датчика, регистрирующего луч, отраженный от кантилевера. Таким образом, использование АСМ микроскопии требует и хорошей настройки оборудования и высокой квалификации научного персонала, при этом квалификация требуется не столько на этапе сканирования, а сколько на этапе обработки и интерпретации результатов.
Прочие методы исследования подобных наносистем либо являются деструктивными, либо существенно опосредованными. На этом фоне стоит обратить внимание на оптические дифракционные методы анализа, именно они, обладая сравнительной экспериментальной и теоретической простотой, позволяют в режиме реального времени получать интегральную информацию о характеристиках регулярной поверхностной структуры.
Рисунок 20 – Разность хода между лучами при падении света под углом и отражении от регулярной структуры под углом
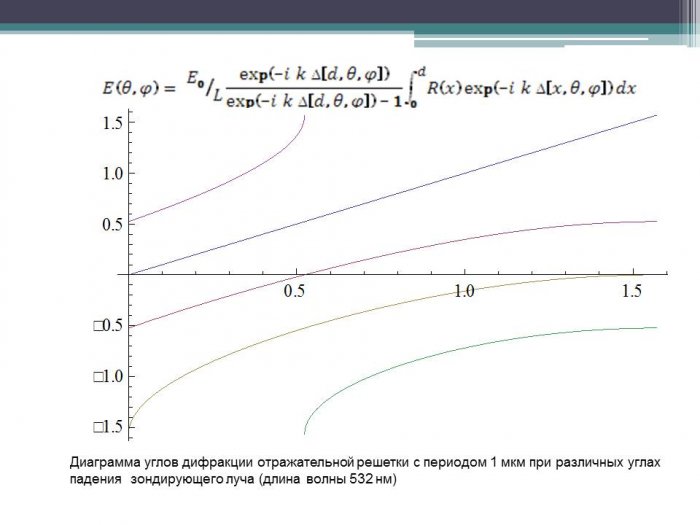
Рассмотрим случай дифракции на одномерной периодической металлодиэлектрической структуре с пространственным периодом d и долей металлического слоя p смотри на рисунок 20. В первом приближении можно считать, что коэффициент отражения от металла близок к 1, а от оксида алюминия – к 0. Тогда, формулируя задачу дифракции в приближении Фраунгофера (параллельные пучки) можно записать
(22)
где k – волновое число;
∆(x)=∆(x,Ɵ,φ)=∆2-∆1=x(sinƟ-sinφ) – локальный набег фазы;
F(x)=R(x)E0/L – напряженность светового поля вторичных источников (отраженного от металла света), где распределение (решетка) коэффициента отражения для отрезка записывается как
, (23)
и для периодично повторяется , – напряженность поля падающей волны, – линейные размеры решетки.
Тогда (1) можно представить в виде суммы интегралов (в случае сумма будет бесконечной)
. (24)
То есть мы заменяем интеграл по N периодам решетки, суммой из N интегралов по каждому из периодов. С учетом условия периодичности решетки можно переписать
С учетом последнего выражения (24) записывается как
откуда
(25)
Рисунок 21 – Диаграмма углов дифракции отражательной решетки с периодом 2 мкм при различных углах падения зондирующего луча (длина волны 532 нм)
Рисунок 22 – Диаграмма углов дифракции отражательной решетки с периодом 1 мкм при различных углах падения зондирующего луча (длина волны 532 нм)
Заключение
В ходе выполнения данной дипломной работы была усовершенствована электролитическая ванна, позволяющая располагать анодируемый образец горизонтально и, тем самым, существенно повышать однородность процесса анодирования и получать образцы сквозного пористого оксида алюминия с более регулярной структурой. Преимуществом установки является то, что она используется как и для анодирования, так и для электрохимического осаждения металла в поры.
Были опробованы различные режимы анодирования и выбраны оптимальные условия, как для сквозного образования пористого оксида алюминия, так и для частичного. Была апробирована методика электрохимического осаждения металла и найдены оптимальные условия заполнения нанопор. В качестве заполнителя использовались медные наночастицы.
В работе, предложена и апробирована технология получения медных наночастиц методом растворения оксидной матрицы содержащей металл. Получено подтверждение наличия медных начастиц спектроскопическими методами и методами методами атомно-силовой микроскопии.
Был предложен метод экспресс-контроля наноструктурированных медных поверхностей, для упрощённого доказательства нахождения наночастиц меди в порах.
Список используемых источников
1 Грибачев, В. А. Компоненты и нанотехнологии / В. А. Грибачев. – СПб.: СПГУТД, 2009. – 107 с.
2 Murray, C.B. Synthesis and characterization of nearly monodisperse CdE semiconductor nanocrystallites / C. B. Murray, D. J. Norris, M. G. Bawendi. – Columbus: 1993. – 115 с.
3 Олейников, В. А. Квантовые точки в биологии и медицине / В. А. Олейников // Природа. – 2010. – № 3. – С. 35–54.
4 Delerue, C. Nanostructures: Theory and Modelling / C. Delerue, M. Lannoo. – Springer, 2004. –305 p.
5 Reed, M. A. Hard skinned aluminium / M. A. Reed, J. N. Randall, R. J. Aggarwal, R. J. Matyi, T. M. Moore, A. E. Wetsel // Phys Rev Lett. – 1988. – P. 535–537.
6 Wang, X Advanced Materials Research / X. Wang, J. Ding, J. Li, H. Jiang // Nature. – 2012. – Vol. 345. – P. 429–434.
7 Chilton, L. V. Aluminium in Electrical Engineering / L. V. Chilton // Nature. – 1957. – 8 june (Vol. 179). – P. 1170–1171.
8 Wood, G. C. Alternating Current Resistivity Profiles Through Anodic Oxide Films on Aluminium and its Alloys / G. C. Wood, A. J. Brock // Nature. –1966. – 19 febr. (Vol. 209). – P. 773–775.
9 Кареев, И. Е. Эндометаллофуллерены / И. Е. Кареев. – М.: МГУ, 2001. – 23 с.
11 Белов, А. Н. Особенности получения наноструктурированного анодного оксида алюминия / А. Н. Белов, С. А. Гаврилов, В. И. Шевяков // Российские нанотехнологии. – 2006. – Т. 1. – № 1–2. – С. 223–227.
12 Белов, А. Н. Факторы, определяющие степень упорядоченности пористого анодного оксида алюминия / А. Н. Белов. – М.: МИЭТ, 2006. – 34 с.
13 Кашкаров, П. К. Увеличение эффективности нелинейно–оптических взаимодействий в наноструктурированных полупроводниках / П. К. Кашкаров, Л. А. Головань, С. В. Заботнов, В. А. Мельников, Е. Ю. Круткова, С. О. Коноров, А. Б. Федотов, К. П. Бестемьянов, В. М. Гордиенко, В. Ю. Тимошенко, А. М. Желтиков, Г. И. Петров, В. В. Яковлев // Физика твердого тела. – 2005. – Т. 47.– вып. 1. – С. 153–159.
14 Оптика наноструктур : учеб. пособие / С. В. Гапоненко, Н. Н. Розанов, У. Л. Ивченко, А. В. Федоров, А. М. Бонч–Бруевич, Т. А. Вартанян, С. Г. Пожибельский.– СПб.: Недра, 2005. – 326 с.
15 Сраго, И. А. Основы электрохимии: текст лекций / И. А. Сраго, Г. С. Зенин. – СПб.: СЗТУ, 2005. – 39 с.
16 Сокол, В. А. Особенности роста пористого оксида алюминия / В. А. Сокол. – Минск: БГУ ИиР, 2003. – 58 с.
17 Паркун, В. М. Исследование объемного роста пленок пористого оксида алюминия / В. М. Паркун, И. А. Врублевский, Е. П. Игнашев, М. В. Паркун. – Минск: БГУ ИиР, 2003.– 47 с.
18 Борисенко, В. Е. Наноэлектроника: учеб. пособие / В. Е. Борисенко, А. И. Воробьева.– Минск: БГУ ИиР , 2003.– 77 с.
19 Аверьянов, Е. Е. Справочник по анодированию / Е. Е. Аверьянов. – М.: Машиностроение, 1988. – 224 с.
20 Грилихес, С. Я. Обезжиривание, травление и полирование металлов / С. Я. Грилихес под ред. П. М. Вячеславова. – 5–е изд., перераб. и доп. – Л.: Машиностроение, 1983.— 101 с.
21 Сокол, В. А. Конструктивно–технологические методы создания гибридных микросхем на основе алюминия и его анодных оксидов: дис. д–ра техн. наук. / В. А. Соколов. – М.: 1988. – 315 с.
22 Попова, С. С. Формирование на сплавах алюминия при анодном оксидировании окрашенных оксидных слоев / С. С. Попова, Е. А. Савельева, О. В. Титоренко. – Киров: 1994. –68 с.
23 Одынец, Л. Л. Анодные оксидные пленки / Л. Л. Одынец, В. М. Орлов. – М.: Наука, 2009. – 200 с.
24 Badellino, F. Anodized Aluminium Grains Labelled with Radiophosphorus for Medical Purposes / F. Badellino, L. Caldarola, G. B. Fasolo, R. Malvano, U. Rosa // Nature. –1964. – 6 June. (Vol. 202). – P. 983–984.
27 O'Sullivan, J. P. One-dimensional polymer based nanocomposites. From tailored fabrication to applications / J. P. O'Sullivan, G.C. Wood // Proc. Roy. Soc, 1970. – Vol. A. 317. – P. 511–543.
28 Денисов, А. И. Оcобенности пористой структуры анодных оксидных пленок на алюминии: В ч. 2. Тонкие пленки и слоистые структуры: материалы междунар. науч.-техн. конф. / А. И. Денисов, Н. М. Яковлева, А. Н. Яковлев. – М.: 2008. – 174 с.
29 Репникова, Е. А. Микропористость оксидных пленок алюминия / Е. А. Репникова, Е. А. Чупахина, Н. М. – Дубна: 2007. – 263 с.
30 Петрова, В. В. Микропористость анодных оксидных пленок алюми- ния: учебное пособие / В. В. Петрова. – Петрозаводск: Изд-во ПГУ, 2009. – 96 с.
31 Францевич, И. Н. Анодные оксидные покрытия на металлах и анодная защита / И. Н. Францевич. – Киев: Наукова думка, 2005. – 280 с.
32 Соколов, В. А. Анодные оксидные пленки / В. А. Соколов. – М.: Наука, 2003. – 215 с.
33 Фролова, О. В. Высокоэффективная одностадийная технология анодирования и окрашивания алюминия его сплавов / О. В. Фролова, Е. А. Савельева // VI Саратовский салон изобретений инноваций инвестиций, СГАУ им. Вавилова. – 2011. – С. 15-16.
34 Su, Z. X. Formation mechanism of porous anodic aluminium and titanium oxides / Z. X. Su, W. Z. Zhou // Adv Mater. – 2008. – Vol. 19– 20. – Р. 136–234 .
35 Sample, C. Formation of porous metal oxides in the and dization process / C. Sample, A.A Golovin // PHYSICAL REVIEW E74. – 2006. – Р. 245–256.
36 Чернякова, К. В. Получение тонких мембран на основе анодного оксида алюминия для пленочных сенсоров / К. В. Чернякова, И. А. Врублевский. – Минск: 2010. – 828 с.
37 Jason, A. C. Effects of Water Vapour on the Electrical Properties of Anodized Aluminium / A. C. Jason // Nature. – 1953. – 24 january ( Vol. 171 ). – P. 177–178.
38 Электрохимическая размерная обработка металлов и сплавов. проблемы теории и практики: монография / О. И. Невский [и др.]. – Иваново: ГОУ ВПО, 2006. – 28 с.
39 Томашов, Н. Д. Толстослойное анодирование алюминия и его сплавов / Н. Д. Томашов, М. Н. Тюкина, Ф. П. Заливалов. – М.: Изд–во Машиностроение, 1968. – 157 с.
40 Кауля, А. Р. Химические методы синтеза неорганических веществ и материалов / А. Р. Кауля. – М.: МГУ им. М. В. Ломоносова, 2008. – 211 с.
ПРЕЗЕНТАЦИИ К ДИПЛОМНОЙ РАБОТЕ
Скачать дипломную работу: