ЦВЕТНЫЕ МЕТАЛЛЫ
В технике наибольшее самостоятельное значение имеют следующие цветные металлы: медь, никель, алюминий, цинк, свинец и олово.
МЕДЬ
В чистом виде медь имеет розовато-красный цвет, почему и называется красной медью.
Чем чище медь, тем розовее ее цвет и мельче сыпь в изломе; чем больше в ней примесей, тем грубее и темнее излом.
Удельный вес чистой меди равен 8,93, температура плавления 1083°, коэфициент линейного расширения при нагреве от 0 до 100° С—16,80*10-6, предел прочности при растяжении 22 кг/мм2 и удлинение 35—50%. Чистая медь обладает высокой электро- и теплопроводностью, очень пластична и хорошо поддается обработке давлением как в холодном, так и в нагретом состоянии. Так как расплавленная медь легко растворяет газы, то литейные качества чистой меди невысоки.
Кристаллическая решетка меди представляет собой куб с центрированными гранями. Аллотропических превращений медь не имеет.
Продажная медь всегда содержит некоторое количество примесей мышьяка, сурьмы, висмута, свинца и железа, а также кислорода в виде закиси меди Сu20; в наиболее чистой меди, полученной путем электролиза, количество примесей снижается до 0,01%.
Примеси сильно влияют на физические свойства меди; это влияние в большинстве случаев вредно. Сурьма и висмут сильно понижают электропроводность и механические свойства меди; особенно вредной примесью является висмут, делающий медь красноломкой при содержании 0,02%, а при 0,05% — хладноломкой. Свинец сообщает меди хладноломкость; содержание его в меди не должно превышать 0,15%. Даже ничтожные количества серы делают медь хрупкой. Мышьяк увеличивает тягучесть меди и сильно уменьшает при этом электропроводность; поэтому присутствия мышьяка избегают, если медь предназначается для электрических проводов, и считают желательной его примесь до 0,35%, если медь идет на изготовление частей топок. Кислород (в виде Сu2O) понижает вязкость меди, а также и ее механические качества, вступая в соединения с веществами, вводимыми в медь для образования сплавов (олово, свинец, алюминий), и разлагаясь при высокой температуре в присутствии водорода с образованием водяного пара, который вызывает в меди трещины.
Содержание в меди Сu2O не должно превышать 1%.
Присутствие в меди Сu2O легко можно установить микроскопическим анализом.
На фиг. 140 дана микроструктура нераскисленной меди, содержащей около 5% Сu2O.
Обработка меди давлением в холодном состоянии (наклеп) сильно изменяет ее механические качества.
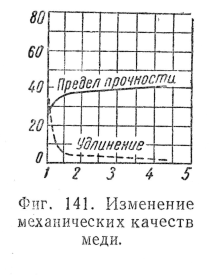
О влиянии холодной обработки на механические качества электролитической меди можно судить по данным диаграммы (фиг. 141); по оси X отложены проценты обжатия испытываемого образца по отношению к первоначальному его сечению, а по оси Y — для кривой предела прочности при растяжении нагрузки в кг, для кривой удлинения — проценты от первоначальной длины образца.
Рассмотрим некоторые из важнейших сплавов меди.
Латуни. Латунями называются сплавы меди с цинком (от 20 до 55% Zn). Цвет сплавов меди с цинком и их механические качества сильно меняются с изменением количества содержащегося в них цинка.
При содержании цинка до 18—20% латуни имеют желтовато-красный цвет; от 20 до 30% — буро-желтый; от 30 до 42% — светло желтый; при 42% — светло-красный, при 50% — золотисто-желтый; при 60% — серебристо-белый; сплавы, содержащие цинка не более 20%, называются томпаком.
Изменение механических свойств латуни в зависимости от количества содержащегося в ней цинка проявляется в возрастании предела прочности при растяжении при увеличении содержания цинка до 45%, после чего предел прочности уменьшается, а также в увеличении относительного удлинения при увеличении содержания цинка до 30%.
Наиболее пластичными будут латуни, содержащие около 30% Zn, а наиболее прочными — содержащие около 45% Zn. Латуни, содержащие 45% Zn, обладают значительной хрупкостью; наиболее широко применяются латуни, содержащие от 28 до 42% цинка.
Обработанная в холодном состоянии латунь приобретает наклеп, для устранения которого ее подвергают отжигу, нагревая в интервале температур от 600 до 700°.
При нагреве до 800 —900° входящий в состав латуни-цинк начинает испаряться, и состав ее изменяется с поверхности, обогащаясь медью. Латунь, содержащая не более 36% Zn, не принимает закалки, при 36% Zn и выше закаливается.
Изменения физических свойств латуни в зависимости от изменения содержания в ней цинка становятся понятными при рассмотрении диаграммы состояния сплавов медь — цинк (фиг. 142).
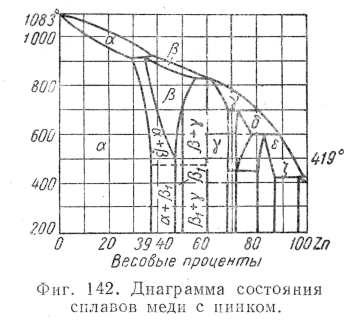
Из диаграммы видно, что сплавы меди с цинком образуют при затвердевании шесть различных твердых растворов — а, в, у, б, е, n, которые при медленном охлаждении подвергаются различным изменениям. Пунктирная линия диаграммы, соответствующая температуре, близкой к 450°, указывает на упорядочение расположения атомов в твердом растворе р, сопровождаемое небольшим выделением тепла. Упорядоченное состояние твердого раствора принято обозначать через в'.
Указанные выше изменения свойств латуни, как видно из диаграммы, соответствуют различным структурам латуни; широкое техническое применение имеют а-латуни, содержащие до 36% Zn и (а + в)-латуни, содержащие
до 45% Zn. Возможность закалки (а + в)=латуни связана с превращениями в-твердого раствора.
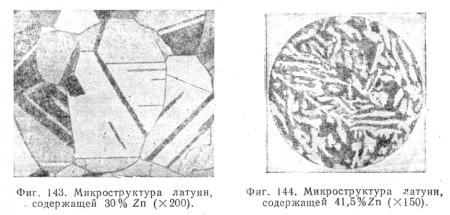
На фиг. 143 показана микроструктура а-латуни, содержащей 30% Zn, подвергнутой холодной обработке и отжигу; на фиг. 144 — микроструктура литой (а + в) = латуни, содержащей 41,5% (зерна a-твердого раствора светлые,
а зерна в-твердого раствора темные).
Для придания латуни специальных свойств в нее вводят специальные примеси (свинец, марганец, олово, никель, железо, алюминий, магний и кремний). На диаграмме состояния действие специальных примесей выражается в различном смещении критических точек и пограничных линий между различными областями диаграммы.
При исследовании сплавов меди с цинком при помощи рентгеновских лучей установлены и пространственные решетки для различных типов латуни.
Бронзы. Бронзами называются сплавы меди с оловом. В последнее время это название дается и медным сплавам, не содержащим олова, если внешний вид и свойства их близки к свойствам сплава меди с оловом (за исключением латуни).
Оловянистая бронза была известна человеку еще в доисторические времена. Сравнительно низкая температура плавления и высокие механические качества делали ее ценным материалом как для изготовления оружия, так и пред
метов домашнего обихода. Вследствие красивого цвета некоторых бронз их применяли и для изготовления художественных изделий. Можно отметить, что состав доисторических и древних бронз исторического периода соответствует наилучшим механическим качествам их как материала, предназначавшегося главным образом для изготовления топоров, мечей, наконечников стрел (около 15% Sn).
В настоящее время для удешевления оловянистой бронзы и для облегчения обработки ее резцом к ней добавляют некоторое количество цинка и свинца. Прибавление к олова изменяет как цвет меди, так и ее физические
свойства.
При содержании в бронзе около 5% олова она имеет желтый цвет, при 10— 12% — оранжевый, начиная приблизительно с 28% — белый.
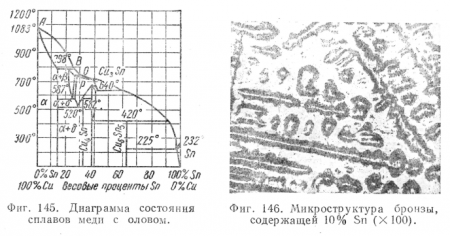
С увеличением содержания олова до 17% увеличивается сопротивление бронзы разрыву; наибольшую твердость имеет бронза, соответствующая химическому соединению Cu3Sn (фиг. 145), содержащая 38,2% Sn. Удлинение увеличивается при повышении содержания Sn до 6%, а затем резко падает, снижаясь при 13% Sn почти до нуля. Бронзы, содержащие не менее 14% олова, приобретают способность принимать закалку. На фиг. 145 дана диаграмма состояния сплавов меди с оловом.
Рассматривая диаграмму, можно получить объяснение отмеченным выше изменениям свойств бронз с изменением содержания олова. Так, при содержании олова выше 13,9% в структуре сплава, помимо кристаллов твердого раствора а, появляются кристаллы твердого раствора о (при низких температурах).
Выше было указано, что приблизительно при этом содержании олова бронза имеет минимум вязкости; кроме того, становится понятным, почему бронзы, содержащие менее 14% олова, неспособны закаливаться. Из диаграммы видно, что превращения в твердом состоянии имеют место только в бронзах, содержащих более 13,9% Sn.
Не следует смешивать с закалкой повышение твердости бронзы, содержащей менее 13,9% Sn, при быстром охлаждении в процессе отливки; в последнем случае повышение твердости происходит вследствие возникающей при этом неоднородности состава кристаллов твердого а-раствора. В результате быстрого охлаждения оси дендриты будут более богаты медью, чем объемы, соответствующие междуосным пространствам. Такое неравномерное распределение компонентов в быстро остывающей бронзе может вызвать местное образование эвтектоида а + б и даже образование кристаллов 8 в структуре бронз,тсодержащих менее 13,9% Sn. Максимальная твердость бронзы, получающаяся при содержании в ней 38,2% Sn, как видно из диаграммы, соответствует образованию химического соединения Cu31Sn,
Диаграмма также дает объяснение, почему происходит умягчение бронзы, содержащей свыше 13,9% Sn после быстрой закалки от температуры, лежащей несколько выше 520°. Из диаграммы ясно, что закалка тормозит выделение твердых и хрупких кристаллов о, входящих в состав эвтектоида а + б, образующегося при 520°.
На фиг. 146 дана фотография микроструктуры литой бронзы, содержащей 10% Sn; на фигуре видно дендритное строение сплава.
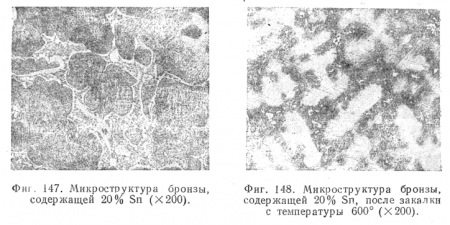
На фиг. 147 дана структура медленно охлажденной бронзы, содержащей 20% Sn: темные участки соответствуют структурной составляющей а, а светлые — эвтектоиду а + б.
На фиг. 148 дана микрофотография структуры той же бронзы, но уже закаленной от температуры ~600°; здесь темные участки соответствуют также структурной составляющей а, а светлые а + б.
АЛЮМИНИЙ
Алюминий — металл белого цвета с голубоватым оттенком; удельный вес — 2,7; температура плавления 660°; коэфициент линейного расширения при нагреве от 0 до 100° — 23* 10-6; предел прочности при растяжении литого алюминия 6—12 кг/мм2 и удлинение около 40%; электропроводность алюминия составляет 60% электропроводности меди. Кристаллическая решетка алюминия —куб с центрированными гранями. Аллотропических превращений алюминий не имеет.
На воздухе алюминий покрывается тонкой пленкой окисла, которая предохраняет его от дальнейшего окисления. Окислы алюминия безвредны. Алюминий растворяется в щелочах и соляной кислоте; серная кислота на него действует слабо, азотная не оказывает почти никакого действия.
Алюминий можно хорошо обрабатывать давлением как в горячем, так и в холодном состоянии, а также резанием.
Несмотря на сравнительно большую линейную усадку (1,7—1,8%), распространены литые изделия из алюминия.
В продажных сортах алюминия общая сумма примесей колеблется в пределах от 0,5 до 2%; главное место среди них принадлежит железу и кремнию.
На фиг. 149 дана микроструктура чистого алюминия. Наклепанный алюминий быстро разрушается под действием речной воды; если наклепанный алюминий подвергнуть отжигу при 450°, то речная вода будет оказывать на него лишь незначительное действие, выражающееся в появлении обычного тонкого слоя окисла на поверхности.
Алюминий и его сплавы применяют для изготовления посуды, листов, труб, электрических проводов, в качестве специальной добавки к сталям, а также в качестве раскислителя при производстве стали.
Важнейшими сплавами алюминия являются силумин и дуралюмин.
Силумин. Силуминами называются сплавы алюминия с кремнием; содержание кремния в таких сплавах колеблется в пределах 11—14%. Силумины отличаются высокими механическими и литейными качествами, их хорошо можно обрабатывать резанием. Наиболее высокие механические качества имеет -эвтектический сплав, содержащий 13,8% Si.
Предел прочности при растяжении силумина около 20 кг/мм2 и удлинение около 10%; он способен сохранять высокие механические качества при нагреве до 300°.
К этому типу сплавов следует отнести и алюминиевокремниевые сплавы, применяемые для отливок под давлением; наиболее употребительный состав их — 86% Аl, 12% Si и 2% Мn.
Дуралюмин. Под названием дуралюмина известен сплав алюминия с медью, вошедший в употребление с 1911 г. Отличительной особенностью этого сплава является самопроизвольное изменение механических свойств после закалки по истечении некоторого времени. Изменение свойств сплава с течением времени без заметного воздействия на него каких-либо внешних факторов принято называть старением сплава.
С течением времени механические свойства дуралюмина изменяются в положительную сторону.
Химический состав дуралюмина приблизительно таков: 2,5—6,0% Сu; 0,25—2,0% Mg; 0,25—2,0% Мn; 0,5% Fe; 0,5% Si; остальное Аl.
В литом виде механические качества дуралюмина мало отличаются от механических качеств чистого алюминия; повышение механических свойств в нем наблюдается лишь после термической обработки, заключающейся в закалке с нагрева до 420—520°; температура нагрева определяется составом сплава. Охлаждение производят в воде, холодной или подогретой, а также в масле. Нагрев выше 550° вызывает пережог.
Тотчас после закалки механические качества дуралюмина невысоки; они начинают повышаться с течением времени и затем делаются постоянными. Повышение механических качеств дуралюмина после закалки в холодной воде при комнатной температуре наблюдается в течение семи суток; некоторое изменение свойств дуралюмина происходит и после этого срока.
Изменение механических свойств дуралюмина в процессе термической обработки и старения характеризуется приблизительно следующими цифрами: в литом виде предел прочности при растяжении 14—18 кг/мм2, при удлинении 3—5%, в прокатанном и отожженном — предел прочности 20 кг/мм2, удлинение 18%, а после термической обработки и старения — предел прочности около 40 кг/мм2 и удлинение около 20%.
Если после закалки дуралюмин будет подвергнут выдержке при повышенной температуре, то процесс старения ускорится. Так, при выдержке после закалки в ванне с кипящей водой дуралюмин приобретает высокие механические свойства через несколько часов (вместо семи суток). Изменение свойств дуралюмина с течением времени может быть объяснено следующим образом. Медь, магний, кремний, входящие в состав дуралюмина, при нагреве до 500° образуют с алюминием твердые растворы; эти твердые растворы при быстром охлаждении фиксируются. Однако такое состояние сплава не является устойчивым, так как растворимость указанных элементов в алюминии при комнатной температуре значительно ниже, чем при 500°. При старении из твердого раствора Сu, Si и Mg начинают выделяться в виде субмикроскопических кристалликов химические соединения (CuAl2, Mg2Si), которые, играя в сплаве роль шипов, увеличивают его крепость (подобно гравию в бетоне).
При выдержке в горячей воде этот процесс выделения происходит легче, и процесс повышения крепости (старения) ускоряется.
Закаленный и состаренный дуралюмин обладает повышенной хрупкостью, поэтому его нельзя подвергать холодной обработке давлением. Для осуществлен ния такой обработки дуралюмин отжигают при 400°.
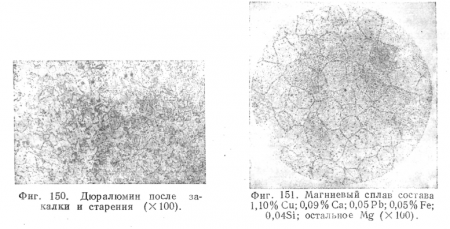
На фиг. 150 представлена микроструктура дуралюмина после закалки и старения.
В России производится дуралюмин, обладающий высокими качествами.
Сравнительно быстрое разрушение алюминиевых сплавов под действием воздуха и влаги несколько ограничивает их распространение.
МАГНИЙ
Магний —металл серебристо-белого цвета; удельный вес 1,74; температура плавления 650°; магний кристаллизуется в гексагональной системе. Чистый магний достаточно стоек в воздухе (почти не уступает алюминию). Раствор поваренной соли, морская вода, кислоты (кроме соляной) быстро разрушают магний; по отношению к щелочам магний стоек. При сгорании магний дает яркий белый свет; магний в 4 раза легче железа, поэтому его сплавы называют сверхлегкими.
В состав промышленных сплавов на магниевой основе могут входить Аl, Zn, Mn, Сu, Si, Cd и другие элементы. Механические свойства чистого магния невысоки, вследствие чего в чистом виде его как конструкционный материал не применяют; в сплавах же на магниевой основе после соответствующей термической и механической обработки достигают предела прочности около 22 кг/мм2 (против — 12 кг/мм2 для чистого магния), удлинение — около 2—5%.
На фиг. 151 дана фотография микроструктуры одного из сплавов магния (1,10% Сu; 0,09% Са; 0,05% Рb; 0,05% Fe; 0,04% Si; остальное Mg).
Скачать реферат:
Пароль на архив: privetstudent.com